Biópsia (coleta de material para exame em laboratório).
Estudo dos pólipos pela colonoscopia.
Tratamento dos Pólipos pela Colonoscopia.
Técnicas usadas para retirar os pólipos por colonoscopia.
Tatuagem do cólon com tinta nanquim.
Complicações da polipectomia e mucosectomia.
Tratamento da hemorragia digestiva baixa (sangramento intestinal).
A colonoscopia é solicitada na suspeita de doenças do reto, cólon e íleo terminal. Solicitado também, para a prevenção do Câncer Colorretal. Permite a biópsia de alterações e a retirada dos pólipos. A maioria dos cânceres de intestino surge dos pólipos (adenoma ou serrilhado) que crescem no intestino e evoluem para o câncer. A lenta evolução dos pólipos, na maioria dos pacientes, permite que a colonoscopia os retire, evitando assim, o aparecimento do câncer e a possibilidade de morte. A colonoscopia encontra pólipos em até 30% das pessoas com 45 anos ou mais.
 Biópsia é um termo usado para descrever a remoção de uma amostra de tecido para enviar ao laboratório de anatomia patológica para análise. Para a biópsia na colonoscopia, uma pinça de biópsia é introduzida por dentro do aparelho até a sua extremidade final, permitindo retirar fragmentos (amostras) do tecido alterado e mesmo quando normal, se a indicação clínica recomendar e enviá-los para a análise em laboratório. As biópsias são usadas para identificar várias condições, mesmo que não se suspeite de câncer. A biópsia é sempre indolor.
Biópsia é um termo usado para descrever a remoção de uma amostra de tecido para enviar ao laboratório de anatomia patológica para análise. Para a biópsia na colonoscopia, uma pinça de biópsia é introduzida por dentro do aparelho até a sua extremidade final, permitindo retirar fragmentos (amostras) do tecido alterado e mesmo quando normal, se a indicação clínica recomendar e enviá-los para a análise em laboratório. As biópsias são usadas para identificar várias condições, mesmo que não se suspeite de câncer. A biópsia é sempre indolor.
|
|
Estudo dos pólipos pela colonoscopia
Uma vez identificado o pólipo, é necessário estudá-lo para definir se é possível a remoção por colonoscopia e qual é a melhor técnica a ser empregada. Avaliar se o aparelho está bem posicionado e de fácil manuseio para o tratamento imediato das complicações. É importante ter em mente os acessórios disponíveis para o procedimento proposto assim como para o tratamento das complicações.
Cromoscopia
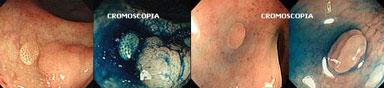
Cromoscopia ou cromoendoscopia do cólon com índigo carmim a 0,2 a 0,5%. Consiste em aplicar um corante pelo canal do aparelho ou por cateter que em contato com a mucosa do cólon melhora a avaliação da superfície permitindo obter informações detalhadas da lesão, assim como do seu tamanho, limites e localização.
Deve ser aplicado com cuidado para não machucar a lesão e causar sangramento, o que dificultaria a avaliação. O corante recomendado no cólon e reto é o índigo carmim a 0,2 a 0,5%. A cromoscopia é usada para caracteriza melhor, delinear e realçar as lesões encontradas durante a colonoscopia. É importante limpar a superfície de lesões suspeitas retirando muco ou resíduos com água e às vezes com mucolíticos (N-acetilcisteína a 10%).
A cromoscopia pode ser utilizada de modo rotineiro, principalmente no ceco e cólon direito, para aumentar a chance de encontrar pólipos e lesões. Portanto, o mérito da cromoscopia é a determinação dos limites exatos da lesão, a visualização de partes ocultas e a demonstração de áreas deprimidas ou elevadas por meio do acúmulo e da distribuição do corante.
A videocolonoscopia convencional, sem magnificação de imagem, mesmo quando realizada por examinador experiente e com emprego de técnica de cromoscopia apresenta capacidade limitada de diferenciação de pólipos colorretais neoplásicos e não-neoplásicos. Quanto à diferenciação de pólipos colorretais benignos e malignos, não ocorreu nenhum caso de “subdiagnóstico. Algumas lesões benignas foram “superdiagnosticados” como malignas, o que, no entanto, não trouxe nenhum prejuízo uma vez que todos foram biopsiados.
Ao contrário da videocolonoscopia com magnificação de imagem, a videocolonoscopia convencional (sem magnificação de imagem) com cromoscopia é um exame diagnóstico de segurança limitada para determinação do diagnóstico histológico de lesões colorretais.
|
|
Magnificação de imagem pela colonoscopia
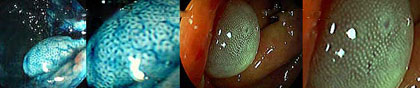
É a capacidade da colonoscopia em ampliar as imagens em tempo real (magnificação) permitindo a visualização de detalhes que não podem ser vistos com a colonoscopia padrão. As imagens podem ser aprimoradas ainda mais pelo uso de corantes (cromoscopia convencional) ou pelo próprio aparelho eletronicamente (cromoscopia eletrônica).
Os colonoscópios de magnificação possuem um mecanismo de foco ajustável que permite imagens endoscópicas padrão e a capacidade de ampliar a imagem de 1,5X a 200X.
O consenso entre observadores da análise da superfície das lesões é alto, mas não deve ser usada para decidir quais lesões colorretais devem ser retiradas ou não, uma vez que não se consegue diferenciar com precisão e segurança necessária as lesões neoplásicas (adenoma e serrilhado) das não-neoplásicas. Além disso, é baixa a capacidade em diferenciar as lesões neoplásicas não invasivas (câncer precoce) das neoplásicas invasivas (câncer avançado).
Os especialistas concordam que a colonoscopia com magnificação é útil, mas não substitui a avaliação histológica (biópsia) das lesões removidas.
|
|
Indicações da cromoscopia na colonoscopia
 A observação endoscópica com cromoscopia pode ser utilizada como método auxiliar em várias situações:
A observação endoscópica com cromoscopia pode ser utilizada como método auxiliar em várias situações:
– Estudo das lesões encontradas na colonoscopia convencional;
– Determinação com segurança das margens das lesões colorretais;
– Pesquisar lesão residual após as retiradas endoscópicas.
– No seguimento dos pacientes com doença inflamatória intestinal (doença de Crohn e retocolite ulcerativa) para avaliar o grau de atividade e prevenção do câncer colorretal.
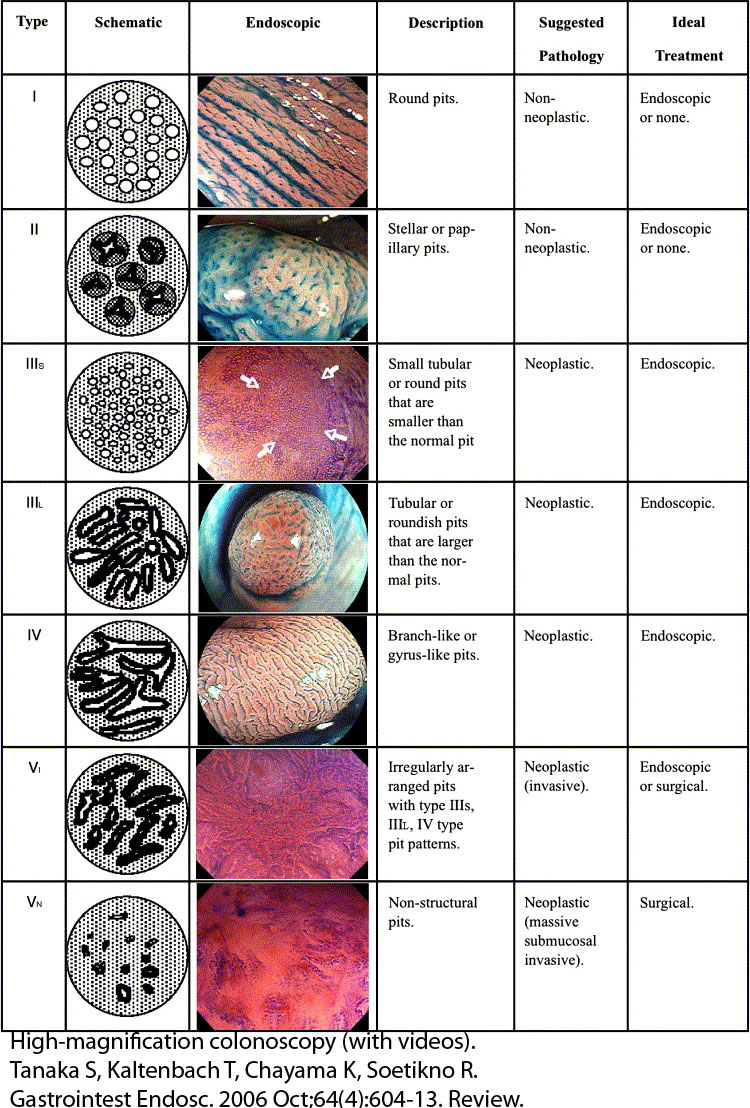
Magnificação de imagem, permite a avaliação dos padrões de criptas da mucosa intestinal (pits), sendo a classificação de Kudo a mais utilizada. A classificação de Kudo subdivide o padrão de criptas em várias categorias (I, II, IIIL, IIIS, IV, Vi (irregular) e Vn (não-estrutural).
.
Todos os pólipos localizados no cólon e reto devem ser retirados pela colonoscopia ou cirurgia. A maioria dos pólipos é retirada pela colonoscopia com baixas taxas de complicações. Recomenda-se que os pólipos menores de 10 mm sejam retirados na introdução do colonoscópio, assim que identificados, porque existe o risco de serem perdidos na retirada do aparelho. A retirada de lesões maiores são trabalhosas e demandam mais tempo quando a injeção constante de ar para manter a luz aberta e retirar o pólipo pode dificultar o término do exame do exame. Para minimizar o risco de perda da lesão e a distensão exagerada do intestino, o local do pólipo pode ser marcado realizando duas biópsias, uma proximal e outra distal a lesão, facilitando a sua identificação e consequente a sua remoção na retirada do colonoscópio. 
|
|
De acordo com revisões sistemáticas e metanálises recentes, adenomas de baixo risco e adenomas avançados de alto risco são perdidos pela colonoscopia com mais frequência do que se acreditava anteriormente.
As perdas chegam a 27% para pólipos serrilhados, 26% para adenomas de baixo risco e 9% para adenomas avançados de alto risco (adenoma tubular ≥ 10 mm; adenoma viloso e displasia de alto grau). As taxas de perda são maiores para adenomas avançados proximais (cólon direito), pólipos serrilhados, adenomas planos e em pacientes com alto risco de câncer colorretal.
As taxas de perda podem ser reduzidas pela preparação adequada do intestino, exame cuidadoso dos ângulos e das pregas intestinais, distensão adequada da luz intestinal e tempo gasto para retirar o aparelho maior que 6 minutos. Atenção a pacientes com múltiplos pólipos e naqueles com histórico de pólipos, porque esses pacientes correm um alto risco de pólipos perdidos na colonoscopia.
Técnicas usadas para retirar os pólipos por colonoscopia
Pólipo séssil com até 3 mm de tamanho
A polipectomia com pinça fria é adequada para lesões com tamanho igual ou inferior a 3 mm. Idealmente, a lesão deve ser completamente envolvida pela pinça, sem tecido sobrando, para que toda a lesão seja removida em uma única mordida. Se ficar tecido residual, mordidas adicionais podem ser realizadas.
A vantagem desta técnica é que uma amostra é sempre recuperada para exame em laboratório. Outra vantagem consiste na não utilização do cautério com risco de sangramento e perfuração desprezíveis.
A desvantagem do uso da pinça é a dúvida sobre a remoção completa do pólipo. Em um estudo, 29% dos pacientes ainda apresentavam tecido neoplásico residual 3 semanas após o tratamento.

|
|
Pólipo séssil entre 3 e 9 mm de tamanho
Polipectomia com alça a frio, sem usar o cautério
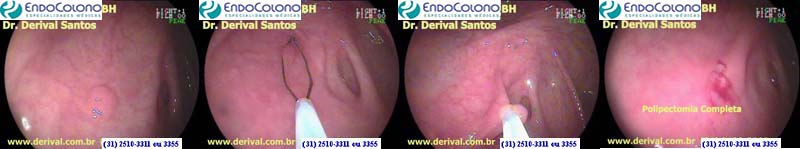
A alça de polipectomia a frio é rápida, eficaz e segura e é a técnica preferida para pequenos pólipos sésseis de até 9 mm de tamanho. Para lesões maiores que 9 mm, pode ser difícil cortar o tecido com a alça sem cauterizar aumentando o risco de sangramento.
Uma alça de polipectomia pequena, mais rígida e fina e com abertura de menos de 12 mm é a ideal. A lesão deve ser colocada na posição das 5 horas, abre-se a alça e circunda o pólipo sem aspiração de ar. Então, a alça captura lentamente o pólipo com pelo menos 1 a 2 mm de tecido normal circundante. O pólipo é cortado, mas não deve ser levantado até que o fechamento da alça seja completo. O pólipo é aspirado através do canal de trabalho para um recipiente.
Taxas zero de perfuração e de menos de 2% de sangramento imediato, sem diferença quando comparado com os retirados com alça com cautério. Este sangramento é discreto e facilmente controlado com técnicas de hemostasia por colonoscopia.
|
|
Polipectomia com alça usando o cautério
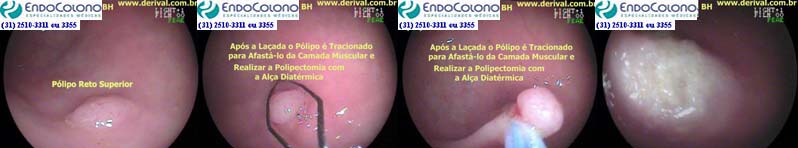
Segue-se o mesmo procedimento descrito no uso da alça a frio, mas no momento de cortar o pólipo, utiliza-se a corrente elétrica produzida pelo cautério.
O cautério pode lesar a parede intestinal em graus variáveis e levar à síndrome pós-polipectomia e mesmo a perfuração. Portanto, deve ser usado com cautela em comparação com a alça a frio. Para minimizar este risco deve-se evitar apreender excesso de tecido normal e o pólipo laçado deve ser afastado da parede do cólon antes da aplicação da corrente elétrica. Atualmente, não há consenso sobre o tipo ideal de corrente que deve ser usado, mas geralmente utiliza-se corrente mista (blend).
|
|
Pólipo séssil maior ou igual a 10 mm e LST (lesão de crescimento lateral)
Ressecção Endoscópica da Mucosa – Mucosectomia
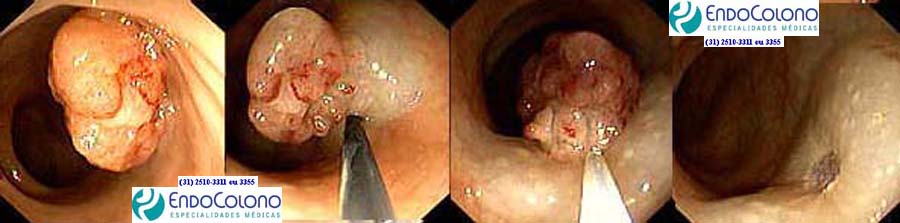
A ressecção endoscópica da mucosa (mucosectomia) é para lesões maiores que 15 mm e recomendado para 10 a 15 mm, mas alguns fazem a frio. Para lesões de 10 a 20 mm consegue-se, na maioria, a retirada em bloco e nas maiores de 20 mm recomenda-se o fatiamento para reduzir o risco de perfuração.
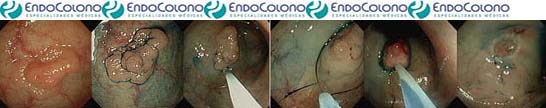
Consiste na injeção de soro fisiológico (NaCl 0,9%) com ou sem adrenalina (1:10.000 a 1:20.000) ou outras soluções abaixo da lesão para levantá-la, criando um plano protetor para colocar a alça de polipectomia e usar com certa segurança a corrente do eletrocautério (mista tipo blend 1). A lógica é facilitar a retirada endoscópica e potencialmente diminuir o risco de perfuração.
O pólipo deve ser orientado na posição das seis horas, que corresponde ao canal de trabalho do endoscópio. O pólipo é laçado e aplicado cauterização para ressecar o tecido.
Geralmente a solução é injetada no centro da lesão ou na borda proximal para que seja exposta. Antes de retirá-lo, é necessário definir as margens da lesão e na dúvida usa-se a cromoendoscopia convencional ou eletrônica com ou sem magnificação.
A falha no levantamento homogêneo da lesão com a injeção da solução suscita preocupação por malignidade, desde que o pólipo não tenha sido submetido a uma tentativa anterior de ressecção (o que poderia resultar em tecido cicatricial fixando a lesão na submucosa).
A injeção submucosa pode ter desvantagens.
—A solução salina é absorvida rapidamente e novas injeções pode dificultar laçar a lesão.
—O líquido injetado pode aumentar a tensão do tecido submucoso e dificultar a captura da alça (isto é, a alça desliza para fora do plano submucoso durante o fechamento).
—O líquido injetado pode se dissipar ao longo do plano submucoso, elevando o pólipo e a mucosa normal adjacente. Isso pode fazer com que o pólipo fique achatado ou deprimido em relação ao tecido circundante.
—A injeção pode deslocar a lesão para um local menos acessível, como atrás de uma dobra, ou contrair a luz, dificultando o acesso.
Após a ressecção, o local da polipectomia deve ter uma superfície “limpa”. A ressecção completa do pólipo em uma única sessão é fundamental, pois as cicatrizes dificultam uma segunda tentativa de ressecção.
|
|
A mucosectomia ideal é a que retira toda a lesão em um fragmento, ou seja, em bloco. As lesões com mais de de 20 mm essa ressecção em bloco pode ser difícil, além de aumentar o risco de complicações, principalmente a perfuração. Para essas lesões maiores de 20 mm, recomenda-se a retirada em fragmentos (mucosectomia a piecemeal).

|
|
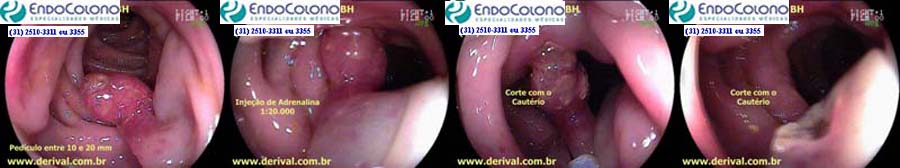
Pólipos pediculados com pedículos com menos de 10 mm de diâmetro
São retirados com a alça de polipectomia usando o eletrocautério pela técnica simples
A técnica padronizada para remover esses pólipos pediculados consiste em abrir alça de polipectomia além da cabeça do pólipo recuando-a lentamente até laçar o pólipo. O pedículo deve ser laçado próximo à sua cabeça, com cuidado para garantir margem de segurança no caso de existir câncer associado e, ao mesmo tempo, um coto do pedículo residual visível que possa ser laçado no caso de sangramento.
Assim que a alça for fechada aplica-se a corrente mista (cauterização blend 1) para evitar o corte a frio e assim, reduzir a frequência de sangramento.
O coto residual do pedículo deve ser revisado alguns minutos após a polipectomia para assegurar a ausência de sangramento. O pólipo é recuperado e enviado para análise. Todo o processo é indolor.
As taxas de sangramento aumentam quando o pedículo é > 5 mm. No entanto, o tamanho para a aplicação de medidas profilática para evitar sangramentos não é conhecido. As diretrizes recomendam que, para um pólipo pediculado com uma cabeça ≥ 20 mm ou um pedículo ≥ 10 mm de diâmetro, usar medidas mecânicas para hemostasia e/ou usar uma injeção de adrenalina diluída.

|
|
Pólipos pediculados com pedículos entre 10 e 20 mm de diâmetro
As diretrizes recomendam que, para um pólipo pediculado com uma cabeça maior ou igual que 20 mm ou um pedículo entre 10 e 20 mm de diâmetro, usar uma injeção de adrenalina diluída profilaticamente.
Utiliza-se a mesma técnica recomendada para os pólipos menores, mas associado à injeção, em sua implantação na parede intestinal, de solução fisiológica (NaCl 0,9%) com adrenalina variando 1:10.000 a 1:20.000 (1 a 2 ml). Recomenda-se laçar o pedículo como descrito para os pólipos menores, mas mantendo o pedículo estrangulado por cerca de 4 a 5 minutos com o intuito de reduzir o fluxo sanguíneo e iniciar a cascata de coagulação e após este tempo procede-se a polipectomia como já descrito. Segue-se os mesmos cuidados após a polipectomia.
|
|
Pólipos pediculados com pedículos maiores de 20 mm de diâmetro
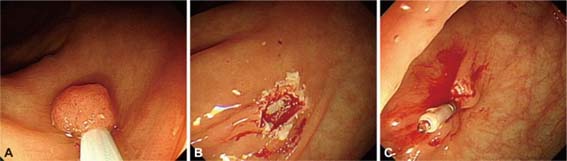
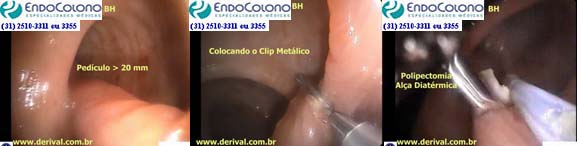
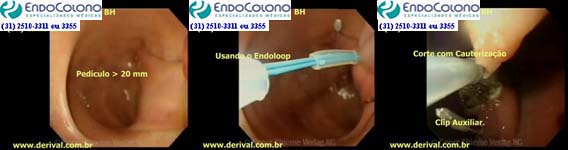
Estudos mostraram que pólipos com pedículos maiores que 20 mm de diâmetro têm um risco maior de sangramento imediato após a retirada (polipectomia). Nesses casos recomenda-se usar métodos profiláticos imediatamente antes da polipectomia para reduzir esse risco. O método ideal é o mecânico através do uso do endoloop (laço oval de nylon destacável) ou clip endoscópico metálico, isoladamente ou em combinação com injeção de adrenalina na base do pedículo. O endoloop e o clip endoscópico ficam presos no local, impedindo o sangramento.
O endoloop é colocado no pedículo do pólipo da mesma maneira que uma alça de polipectomia, mas depois de apertado é solto ao redor do pedículo. No entanto, existem problemas com os endoloops, como, por ser flexíveis, ter dificuldade em laçar o pólipo ou estrangular adequadamente, quando o sangramento imediato pode ocorrer. Sendo assim, o corte do pólipo com o eletrocautério deve ser realizado alguns minutos após o endolop ser apertado, tempo necessário para que o endoscopista perceba a alteração da cor da cabeça do pólipo de vermelho vivo para violáceo, demostrando diminuição significativa do fluxo de sangue.
Um ou mais clipes endoscópicos são colocados na base do pedículo imediatamente antes da polipectomia. A principal vantagem dessa abordagem é que os clipes endoscópicos geralmente são fáceis de colocar. As desvantagens incluem a frequente necessidade de usar vários clipes nos pedículos muito grandes e, de fato, pode ser inviável quando os clipes endoscópicos podem não ter tamanho suficiente para pegar todo o pedículo, mesmo quando vários clipes são aplicados. Outra desvantagem é o processo inflamatório que pode surgir em torno dos clipes que não caem dificultando a diferenciação com pólipo residual nas colonoscopias de controle.
|
|
Pólipos pediculados com a cabeça grande, maior que 25 mm
Quando identificado na introdução do colonoscópio, recomenda-se injetar em sua cabeça, solução com adrenalina variando 1:10.000 a 1:20.000. Reduz o fluxo de sangue e consequentemente o seu tamanho.
Na retirada do colonoscópio, quando provavelmente o pólipo já tenha ficado menor, realiza-se a polipectomia com ou sem a medidas profiláticas de sangramento usando o endoloop (laço oval de nylon destacável) ou clip endoscópico metálico, isoladamente ou em combinação com injeção de adrenalina na base do pedículo. Dependerá do julgamento do médico examinador.

|
|
Lesões Superficiais do Cólon
As lesões superficiais do cólon são as lesões nas quais o comprimento lateral e maior que a altura da lesão. Classificadas de acordo a sua forma em: superficialmente elevadas, deprimidas e de crescimento lateral.
O risco de evoluir para câncer é maior quando comparado a lesões elevadas (pediculada e séssil), mas o diagnóstico é mais difícil. Portanto, a identificação dessas lesões tem importância fundamental para a prevenção do câncer colorretal.
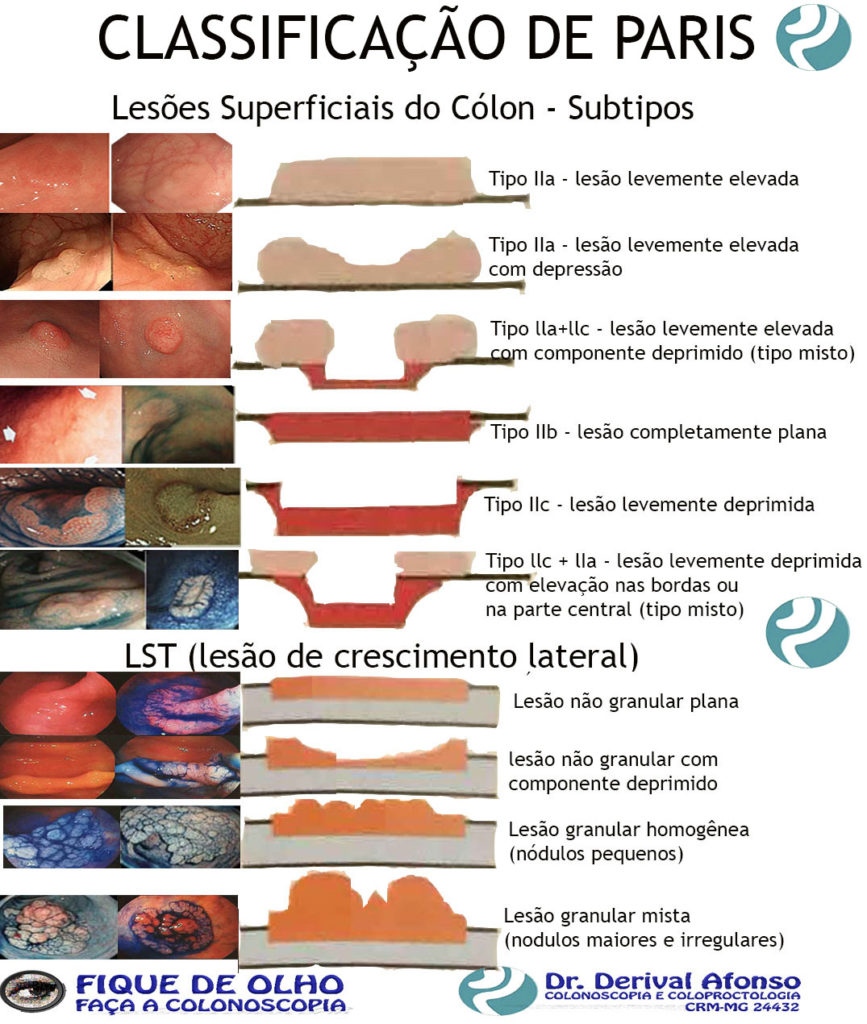 Classificação de Paris
Classificação de Paris
ᴥ» Tipo IIa – lesão levemente elevada;
ᴥ» Tipo IIb – lesão completamente plana;
ᴥ» Tipo IIc – lesão levemente deprimida;
ᴥ» Tipo III – lesão ulcerada;
ᴥ» Tipo lla+llc – lesão levemente elevada com componente deprimido (tipo misto);
ᴥ» Tipo llc + lIa – lesão levemente deprimida com elevação nas bordas ou na parte central (tipo misto). Lesões planas elevadas (IIa) e lesões sésseis (Is) podem ser confundidas. A diferenciação se faz medindo a altura da lesão com a pinça de biópsia fechada, quando for mais elevada que pinça, isto é, maior que 2,5 mm é considerada séssil.
ᴥ» LST (lesão de crescimento lateral) – Considerada quando a lesão superficialmente elevada é maior que 10 mm. São classificadas em:
♦Lesão granular homogênea (nódulos pequenos);
♦Lesão granular mista (nodulações maiores e irregulares);
♦Lesão não granular plana;
♦Lesão não granular com componente deprimido.
Técnicas endoscópicas recomendadas para a retida (ressecção) das lesões superficiais do cólon
Tipo IIa menores que 2 cm. Tipo IIb menores que 1 cm
É usado a mesma técnica recomendada para os pólipos sésseis (alça de polipectomia a ᴥ» ᴥ» frio ou com eletrocautério ou a mucosectomia).
Tipo IIc, IIc+IIa e IIa+IIc menores que 1 cm
É usado sempre a técnica da mucosectomia em bloco (único fragmento). Exceto quando faltar a elevação da lesão ou a elevação da lesão for disforme com a injeção na submucosa (abaixo da lesão). Isso sugere câncer invasivo e impede o tratamento endoscópico. Nesse caso, faz-se a tatuagem alguns centímetros distais com tinta nanquim.
Tipo III – são lesões escavadas, isto é, do tipo ulcerado.
Apresentam uma alta incidência de câncer invasivo, independentemente do tamanho. Exceto quando faltar a elevação da lesão ou a elevação da lesão for disforme com a injeção na submucosa (abaixo da lesão). Isso sugere câncer invasivo e impede o tratamento endoscópico. Nesse caso, faz-se a tatuagem alguns centímetros distais com tinta nanquim.
LST (lesão de crescimento lateral)
A técnica de remoção, por colonoscopia ou por cirurgia, depende do tipo da lesão, da disponibilidade do serviço e da experiência da equipe.
Lesão entre 10 e 20 mm de tamanho
Ressecção endoscópica da mucosa (mucosectomia) em bloco único (EMR). Apenas quando o estudo da lesão pela cromoscopia com ou sem magnificação conseguir descartar áreas de câncer e a mesma se elevar por completo e de forma homogênea, após a injeção de solução na submucosa, sugerindo ausência de câncer invasivo.
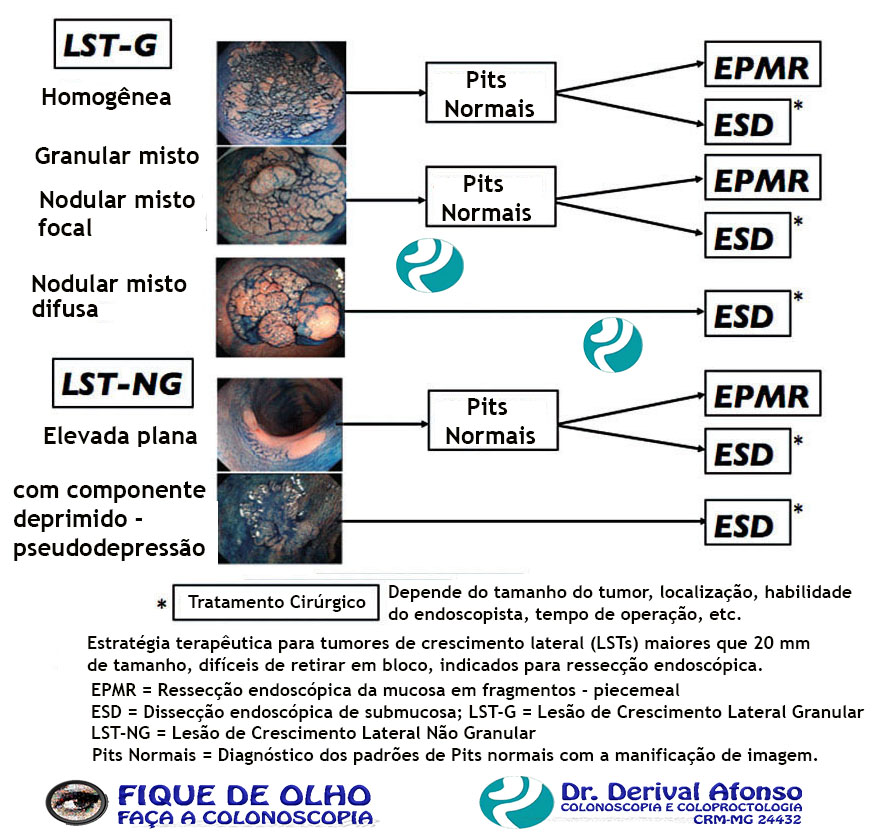 Lesão maior que 20 mm de tamanho
Lesão maior que 20 mm de tamanho
Ressecção endoscópica da mucosa em fragmentos – piecemeal – (EPMR) ou dissecção endoscópica de submucosa (ESD). O tamanho e forma da lesão, a experiência do endoscopista e o material disponível definem qual tipo de técnica usar.
Embora a ESD tenha um tempo de procedimento mais longo e uma maior taxa de perfuração, o seu uso fornece, frequentemente, uma ressecção em bloco.
No entanto, a técnica EPMR é considerada uma opção válida para ressecção de grandes lesões, uma vez que a ESD é pouco disponível. Na EPMR a presença de lesão residual (retirada incompleta) é de 16 % (geralmente uniforme e diminuto), enquanto a recorrência tardia é de 4%. Em ambos os casos se consegue o tratamento endoscópico em 93% dos casos.
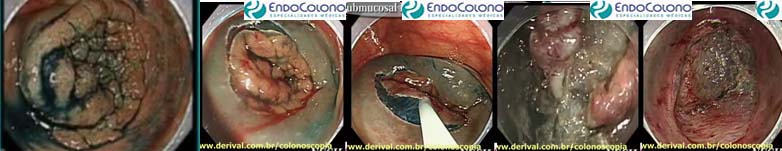
Dissecção endoscópica de submucosa (ESD)
Permite a retirada de grandes lesões em bloco, através da criação de um plano na submucosa (camada entre a lesão de mucosa e a camada muscular). Esse plano é criado com a injeção de solução salina fisiológica (NaCl 0,9%) seguido da injeção da solução de absorção lenta como o HPMC (hidroxipropilmetilcelulosa) ou manitol, misturado com uma pequena quantidade de índigo carmim e adrenalina.
O corante índigo carmim facilita a visualização da camada submucosa e a adrenalina reduz o sangramento durante o procedimento. Um “cap” transparente é acoplado na ponta do endoscópio para ajudar na exposição durante o procedimento.
Inicia-se com a marcação da área ao redor da lesão através de pequenos pontos com o eletrocautério e assim delimitar os limites de ressecção embora alguns profissionais não a utilize. Na maioria dos casos, a incisão da mucosa é iniciada a partir da extremidade mais distante, para determinar o limite distal de ressecção.
Para usar a vantagem da gravidade, alterna a posição do paciente. Alterna-se a utilização dos acessórios de acordo com a necessidade durante o procedimento até a completa ressecção de lesões de praticamente qualquer tamanho.
Acessórios usados:
ᴥ» Para dissecção: I-T Knife II, Hook knife e Flex-knife;
ᴥ» Para hemostasia: pinça hemostática e HemoClips;
ᴥ» Para manter o cólon e reto distendido: bomba de CO2;
ᴥ» Para produzir a corrente de corte: bisturi elétrico de alta frequência com a função endocut o que propicia uma corrente pulsátil.
ᴥ» Para o colonoscópio: cateter injetor de água externa preso na ponta do aparelho por um “cap” transparente.
|
|
Tatuagem do cólon com Tinta Nanquim (tinta da índia)
A tatuagem consiste na injeção de um agente de coloração permanente na parede intestinal para criar uma marca que identificará o local de dentro ou de fora da luz; normalmente é feito com pelo menos duas injeções de corante nos lados contralaterais do intestino próximo à lesão.
A tatuagem deve ser realizada alguns centímetros distais à lesão. As duas principais indicações são:
ᴥ» Para marcar o local da retirada do pólipo, se não tiver certeza de que a remoção foi completa ou se serão necessárias outras sessões para removê-lo, se houver indicadores suspeitos de malignidade e para o controle de recidiva do pólipo, principalmente a retirado em mais de um fragmento (piecemeal).
ᴥ» Para identificar o local da lesão durante a cirurgia aberta e principalmente na laparoscópica e robótica (quando se perde o poder da palpação). A localização durante a cirurgia de lesões detectadas pela colonoscopia é imprecisa, quando se baseia na descrição da colonoscopia, levando em último caso, a não ressecção do segmento apropriado. No entanto, se a lesão estiver localizada no reto, no ceco ou próximo à válvula ileocecal, o local não precisa ser tatuado.
Cateter injetor – Produto tradicionalmente disponível para a injeção de outras soluções como de adrenalina ou ethamolin. Introduzido pelo canal de trabalho do aparelho, tem calibre ideal entre 23 – 25 G, com ponta de 3 – 5 mm.
Recomenda-se uma injeção dupla, com uma solução salina na submucosa para formar uma bolha, seguida de uma injeção de cerca de 1 ml da tinta nanquim esterilizada 1 a 5 % usando uma segunda seringa e completado com mais 1 a 2 ml de solução salina. Parece que esta técnica pode melhorar a eficácia da tatuagem e prevenir complicações inflamatórias e injeção na cavidade abdominal.
|
|
Complicações da polipectomia e mucosectomia
Geralmente são seguras quando realizadas por médico treinado e experiente. Complicações relacionadas: hemorragia, perfuração e a síndrome pós-polipectomia.
Hemorragia (sangramento)
A hemorragia é a complicação mais comum. O risco de sangramento é em torno de 1,7%. O sangramento pode ser imediato, imediatamente após (1,5%) ou tardio, ocorre em média 7 a 12 dias depois (2%). O sangramento varia de discreto em lençol a intenso e arterial, na forma de jato.
O risco está relacionado ao tipo e tamanho do pólipo, à técnica da polipectomia e ao status da coagulação do paciente. Em ambos os casos o tratamento endoscópico é o recomendado e consegue-se controlá-lo em quase todos os casos, sendo a cirurgia raramente necessária.
Tratamento pela colonoscopia no sangramento imediato após a retirada do pólipo
O sangramento imediato ocorre em 1,5% a 2,8% após polipectomia. O risco aumenta quando se descuida da técnica como usar uma corrente de corte muito forte e / ou ao fechar a alça muito rápido. Idade ≥65 anos, doença renal crônica ou cardiovascular, uso de anticoagulantes, pólipo maior que 1 cm de tamanho, morfologia do pólipo, mau preparo intestinal.
O sangramento mais imediato pode ser controlado com várias técnicas endoscópicas. A técnica depende da gravidade do sangramento, do tipo de pólipo e da preferência individual. Uma combinação de técnicas de hemostasia é frequentemente realizada.
Aplicação de pressão
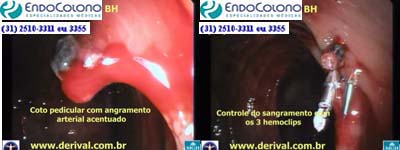
Especialmente para pólipos pediculados, o sangramento imediato após a polipectomia pode ser facilmente interrompido através do controle do pedículo com a alça de polipectomia apertando o pedículo restante interrompendo o fluxo sanguíneo. Após a parada completa do sangramento ativo, outras técnicas devem sem usadas para reduzir o risco de novo sangramento como a cauterização bipolar, injeção de adrenalina ou uso do clip endoscópico.
Injeção com adrenalina
Uma diluição de epinefrina a 1: 10.000 é comumente usada, que é simplesmente injetada na área com sangramento. A injeção da adrenalina é frequentemente complementada com o clip endoscópico.
Cautério
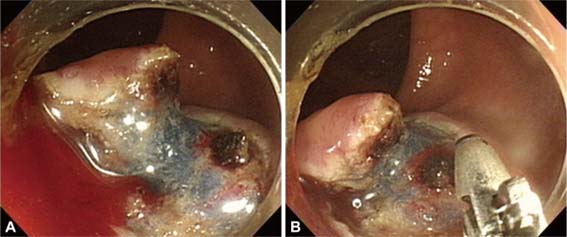 A cauterização é um método eficaz para tratar um local de sangramento. É feito com sondas térmicas, cauterização bipolar ou a ponta de uma alça de polipectomia. Como a parede do cólon é muito fina, a corrente deve diminuir em aproximadamente 50% em relação à usada no trato gastrointestinal superior. Para sonda de calor, 15 J é seguro e 10 a 15 W para cautério bipolar. Ao aplicar com sondas térmicas ou cautério bipolar, os endoscopistas não devem pressionar os dispositivos contra a lesão, o que aumenta o risco de perfuração.
A cauterização é um método eficaz para tratar um local de sangramento. É feito com sondas térmicas, cauterização bipolar ou a ponta de uma alça de polipectomia. Como a parede do cólon é muito fina, a corrente deve diminuir em aproximadamente 50% em relação à usada no trato gastrointestinal superior. Para sonda de calor, 15 J é seguro e 10 a 15 W para cautério bipolar. Ao aplicar com sondas térmicas ou cautério bipolar, os endoscopistas não devem pressionar os dispositivos contra a lesão, o que aumenta o risco de perfuração.
Clip endoscópico é um método seguro e eficaz para tratar sangramentos imediatos. Às vezes é difícil abordar uma lesão com clipes devido à localização. Estudo revelaram que são necessários uma média de 3 clipes para parar o sangramento completamente.
Endoloop e ligadura elástica
O sangramento pós-polipectomia imediato e tardio pode ser tratado com alças de endoloop ou ligadura da banda. Ao usar a ligadura de banda, deve-se evitar alta pressão de sucção para evitar perfuração.
|
|
Tratamento pela colonoscopia do sangramento tardio após a retirada do pólipo.
O sangramento tardio ocorre em até 2% dos pacientes que fizeram a polipectomia. Os sangramentos tardios se desenvolvem em média 5 a 7 dias após a polipectomia, mas podem ocorrer até 30 dias depois.
O tamanho do pólipo está relacionado ao risco de sangramento tardio de 1% para pólipos com menos de 10 mm a 6,5% para aqueles com mais de 20 mm. Idade avançada, hipertensão, pólipos sésseis grandes, pólipos no cólon direito e polipectomia com coagulação pura são conhecidos como fatores de risco para sangramento tardio. Anti-inflamatórios não esteróides ou aspirina não aumentam o risco de sangramento tardio.
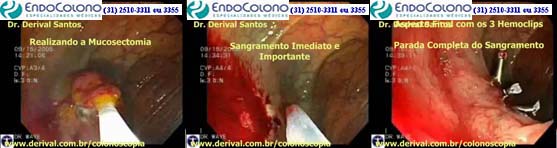
A maioria dos sangramentos pós-polipectomia tardios podem ser tratados com sucesso com técnicas pela colonoscopia. Cerca de metade dos pacientes que são admitidos no hospital com sangramento intestinal dentro de 6 horas a 14 dias após a polipectomia requerem transfusão de sangue. O momento da intervenção depende da quantidade e da taxa de sangramento. A colonoscopia deve ser realizada imediatamente em pacientes com sangramento ativo. Injeção de adrenalina, terapia com eletrocautério ou clips endoscópcicos geralmente são realizados isoladamente ou em combinação.
SANGRAMENTO TARDIO APÓS-MUCOSECTOMIA – TRATAMENTO COM CLIP
|
|
Perfuração
A perfuração ocorre em 0,04% -2,1% quando se retira os pólipos (polipectomia ou mucosectomia).
Pode ser imediata ou tardia.
1- A perfuração imediata é causada por lesão de toda a parede do cólon ao retirar o pólipo.
2- A perfuração tardia ou em segundo tempo se deve a isquemia (falta de sangue) de toda a parede do cólon, ocorre em algumas horas ou dias após a retirada do pólipo.
A maioria das perfurações ocorre após a mucosectomia ou polipectomia de pólipos sésseis e subpediculados.
Dor abdominal associado a sinais de irritação peritoneal (piora da dor a qualquer atividade que mova ou tencione o abdome) após a retirada do pólipo é motivo de investigação imediata. Se o RX simples ou tomografia computadorizada do abdome mostrar ar livre (peumoperitôneo) confirma a perfuração, quando a cirurgia de urgência é mandatória.
Não se pode perder tempo, caso o médico considere a perfuração de vulto, por exemplo, através da visualização da cavidade abdominal ou de órgãos intra-abdominal, e a considera intratável por via colonoscópica.
Algumas perfurações podem ser fechadas imediatamente com clip endoscópico, nesses casos o paciente é internado e a cirurgia adiada. O paciente fica em jejum absoluto com antibióticos e soro por via intravenosa, as vezes usa-se sonda nasogástrica descompressiva, associado à observação clínica e laboratorial (leucograma e PCR) e acompanhado pelo cirurgião.
Com base em pesquisa disponível, na presença de ar livre abdominal (intraperitoneal ou retroperitoneal) sem notáveis sinais clínicos irritação peritoneal (“perfuração silenciosa”), a cirurgia pode ser adiada e com as mesmas medidas clínicas de quando se coloca o clip. As pequenas perfurações podem fechar espontaneamente sem a necessidade de terapia adicional invasiva.

|
|
Síndrome de coagulação pós-polipectomia
A síndrome de coagulação pós-polipectomia (também conhecida como síndrome pós-polipectomia, síndrome de eletrocoagulação pós-polipectomia e síndrome de queimadura transmural) refere-se ao desenvolvimento de dor abdominal localizada, febre e leucocitose (aumento dos leucócitos no sangue) na ausência de perfuração intestinal após a retirada de pólipos com eletrocautério.
O reconhecimento da síndrome de coagulação pós-polipectomia é importante para evitar cirurgia desnecessária, uma vez que o tratamento clínico é eficaz em quase todos os pacientes.
Ocorre em menos de 0,5% das colonoscopias com retirada de pólipos com eletrocautério. Fatores associados ao risco aumentado da síndrome:
ᴥ» Tamanho do pólipo – Quanto maior o pólipo (≥ 10 mm), maior o risco da síndrome;
ᴥ» Forma do pólipo – Lesão não polipóide tem um maior risco síndrome;
ᴥ» Localização da lesão – Lesões no cólon ascendente e no ceco parecem ter taxas mais altas de complicações, incluindo a síndrome pós-polipectomia, e isso se deve a espessura da parede intestinal ser menor;
ᴥ» Pacientes com hipertensão arterial – O risco é maior nos pacientes hipertensos.
Algumas técnicas endoscópicas podem reduzir o risco da síndrome de coagulação pós-polipectomia:
ᴥ» Tracionar o pólipo em direção ao centro da luz, imediatamente antes da aplicação do eletrocautério, para que a mucosa seja afastada do restante da parede intestinal;
ᴥ» Injetar de solução na submucosa para pólipos ≥ 10 mm;
ᴥ» Usar com mais frequência a polipectomia com alça a frio, sem usar o eletrocautério. Dados disponíveis sugerem ser uma opção segura e eficaz, mesmo para para lesões > 10 mm, localizadas no cólon direito e ceco.
Apresentação clínica
Tipicamente apresentam sintomas nas próximas 12 horas após a colonoscopia, mas podem ocorrer até sete dias depois. A maioria dos pacientes apresenta dor abdominal generalizada ou localizada na região do local da polipectomia. Febre e/ou taquicardia também podem estar presentes. O exame abdominal pode revelar sensibilidade abdominal localizada no local da polipectomia, mas alguns podem apresentar sinais e sintomas semelhantes a perfuração intestinal.
Diagnóstico
Deve-se suspeitar da síndrome de coagulação pós-polipectomia nos pacientes que apresentam dor e sensibilidade abdominal após a polipectomia com eletrocautério, particularmente após a remoção de pólipo grande (ou seja, ≥ 10 mm). Pode ser acompanhada por febre, taquicardia e leucocitose.
A tomografia computadorizada do abdome e da pelve (com contraste oral solúvel em água e contraste intravenoso) exclui a perfuração do cólon (ausência de ar livre no abdome). Podem ter espessamento focal da parede do cólon e/ou alteração da densidade da gordura em torno do cólon.
Para pacientes selecionados (por exemplo, aqueles com dor abdominal localizada leve, sem febre e sem taquicardia), pode ser razoável fazer o diagnóstico com base na apresentação clínica e sem exames complementares.
Tratamento
Pacientes selecionados podem ser tratados em regime ambulatorial se todas as condições a seguir forem atendidas:
ᴥ» Dor abdominal leve.
ᴥ» Pressão arterial, frequência cardíaca e respiratória normais e afebril.
ᴥ» Tomografia computadorizada abdominal e pélvica não mostra sinais de perfuração ou outras complicações graves.
O tratamento ambulatorial
Consiste no antibiótico oral por sete dias e uma dieta sem resíduos. Os pacientes são reavaliados clinicamente em dois a três dias. Se os sintomas melhorarem (por exemplo, sem dor abdominal ou febre), a dieta é liberada. Se a condição do paciente não melhorar ou piorar, a internação é necessária.
Antibiótico Oral
A queimadura da parede intestinal pode causar ruptura na barreira de defesa. Devem cobrir a flora gastrointestinal usual, bastonetes gram-negativos e anaeróbios.
ᴥ» Ciprofloxacino (500 mg de 12/12 horas) com metronidazol (500 mg de 8/8 horas).
ᴥ» Levofloxacino (750 mg ao dia) com metronidazol (500 mg de 8/8 horas).
ᴥ» Amoxicillina-clavulanato (875 mg amoxicillina e 125 mg clavulanato) de 8/8 horas. Dieta Dieta sem resíduos até que possam ser reavaliados em dois ou três dias. A dieta pode então ser liberada para uma dieta regular se melhorar clinicamente (sem dor ou sensibilidade abdominal).
Tratamento hospitalar
A hospitalização é necessária para os demais pacientes.
Dieta
Depende da gravidade dos sintomas, jejum (repouso intestinal completo) ou dieta sem resíduos. A resolução da dor abdominal ocorre em dois a três dias, quando a dieta é progredida.
Antibióticos venosos
A escolha depende da gravidade da doença. Metronidazol 500 mg IV cada 8 horas + Ceftriaxona 2g IV uma vez ao dia ou Cefotaxima 2g IV a cada 8 horas ou Ciprofloxacina 400 mg IV a cada 12 horas ou Levofloxacina 750 mg IV uma vez ao dia. Os antibióticos intravenosos devem ser continuados até que a dor abdominal desapareça, geralmente de dois a três dias, quando troca para antibióticos orais (por exemplo, ciprofloxacina com metronidazol ou monoterapia com amoxicilina-clavulanato), para completar um curso de sete.
Cuidados subsequentes
Pacientes com melhora clínica podem receber alta com antibióticos orais para completar um curso de sete dias. Critérios para a alta hospitalar: ᴥ» Normalização dos sinais vitais (isto é, resolução da febre, taquicardia e normalização da pressão arterial). ᴥ» Resolução de dor abdominal. ᴥ» Tolerância a dieta oral.
Pacientes que não melhoram
Se o paciente não melhorar ou piorar (por exemplo, aumento da dor abdominal ou leucocitose, ou desenvolvimento de peritonite difusa), é urgente a avaliação da cirurgia e nova tomografia computadorizada do abdome e da pelve é feita. Se houver suspeita de perfuração do cólon com base no exame clínico (por exemplo, defesa abdominal e rigidez) e/ou exames de imagem mostrando ar extraluminal, o tratamento é direcionado para a perfuração do cólon.
Introdução
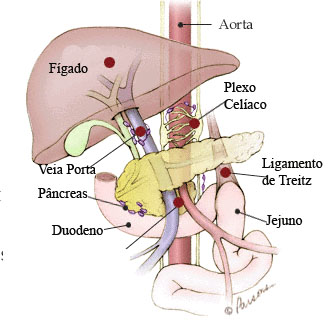 É o sangramento no trato digestivo que se origina abaixo do ângulo de Treitz (junção do duodeno com o jejuno). A saída de sangue vermelho vivo sem fezes através do ânus (enterorragia) tem sua origem no cólon, reto ou ânus em 85 a 90% dos casos.
É o sangramento no trato digestivo que se origina abaixo do ângulo de Treitz (junção do duodeno com o jejuno). A saída de sangue vermelho vivo sem fezes através do ânus (enterorragia) tem sua origem no cólon, reto ou ânus em 85 a 90% dos casos.
Predomina na terceira idade (acima dos 60 anos). Em cerca de 10% a origem não é encontrada.
ᴥ» Abaixo dos 60 anos: Doença diverticular do cólon; Doença inflamatória intestinal; Neoplasia; Ectasia Vascular. ᴥ» Acima dos 60 anos: Doença diverticular do cólon; Ectasia Vascular; Neoplasia.
Exame Clínico
História, exame clínico (frequência cardíaca, pressão arterial e cor das mucosas) e exame proctológico. Afasta doenças anorretais (neoplasias e orificiais – hemorroidas responde por 9% das causas) e também para confirmar o aspecto do sangramento relatado pelo paciente. A retossigmoidoscopia rígida pode ser realizada nos quadros estáveis, mas não elimina a necessidade de outros exames.
Exames Laboratoriais
Tipagem sanguínea, hemoglobina, hematócrito, uréia, creatinina, eletrólitos, glicemia atual e em jejum, coagulograma (TP, TTPA) e gasometria arterial. OBS: Hemoglobina imediata é de valor limitado na hemorragia aguda, pois são necessários de 24 a 48h para o organismo equilibrar o volume intravascular. Hemograma e coagulograma frequentes para avaliar necessidade de hemotransfusões e correção de coagulopatias.
Medidas Iniciais
ᴥ» A prioridade é garantir as vias aéreas pérvias.
ᴥ» Punção venosa no membro superior para coleta de sangue e infusão de soro fisiológico ou Ringer lactato e de concentrado de hemácias (hemotransfusão). O volume a ser infundido depende da perda estimada de sangue, da condição clínica e história de doença cardiovascular incluindo insuficiência cardíaca congestiva.
ᴥ» Correção da coagulopatia (RNI>1,5 – transfusão de plasma fresco e aqueles com contagem de plaquetas < 50.000 – transfusão de plaquetas) e dos distúrbios eletrolíticos se presentes.
ᴥ» Após 24 a 48 horas, com o equilíbrio do volume intravascular, o valor do hematócrito reduz-se. O hematócrito reduz-se aproximadamente 2 ou 3 pontos e a hemoglobina 1 ponto para cada 500 mililitros de sangue perdido. O objetivo é manter o hematócrito igual ou maior que 30 nos idosos e igual ou maior que 20 nos jovens saudáveis. ᴥ» A elevação da uréia/creatinina pode indicar gravidade do sangramento por refletir a intensidade da perda sanguínea e risco de insuficiência real aguda.
ᴥ» Sondagem gástrica para ver o conteúdo, quando não apresentam hematêmese (vômitos de sangue) e têm dificuldade de acesso à endoscopia para afastar origem gastroduodenal.
ᴥ» Acesso venoso central puncionando a veia jugular interna: para auxiliar a reposição volêmica e proporcionar a verificação periódica da pressão venosa central (PVC) nos casos de sangramento maciço e/ou instabilidade hemodinâmica
ᴥ» Colocação de cateter vesical: nos pacientes com choque hipovolêmico, para monitorar a resposta da reposição de fluídos por meio da perfusão renal.
Colonoscopia
A colonoscopia é o exame inicial de escolha na investigação e tratamento em pacientes com hemorragia digestiva baixa aguda moderada e maciça.
A acurácia diagnóstica varia de 72% a 86% com morbidade de 0,3%. O preparo de cólon anterógrado (via oral) é o método de eleição por ser fácil, útil e não causar ressangramento ou aumentar a velocidade do mesmo. Geralmente utiliza-se 50 a 75% da dose usual pelo sangue na luz intestinal ser um laxante natural.
O melhor momento para realizar a colonoscopia é em 12 a 24 horas após a chegada no hospital. Embora a colonoscopia de urgência realizada nas primeiras 12 horas seja segura e eficiente, e está relacionada à redução do tempo de internação e diminuição dos custos hospitalares.
Para a maioria dos profissionais a colonoscopia deve ser realizada assim que as condições clínicas, após as medidas iniciais, permitirem. Quando o sangramento é muito importante e não se consegue compensar adequadamente o paciente a colonoscopia deve ser realizada no CTI com o paciente intubado e 1 hora após o término do preparo de cólon através da sonda gástrica associado a 1000 ml de clister glicerinado.
Tratamento endoscópico na hemorragia digestiva baixa cólica
Métodos de tratamento endoscópico da hemorragia digestiva colorretal
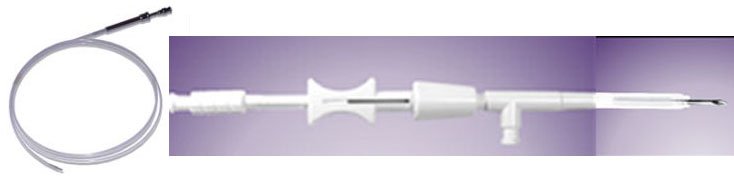
1- Terapia com Infiltração: adrenalina, etanolamina e álcool absoluto Agulha de esclerose para colonoscopia com cateter em teflon e ponta afilada e sistema de manopla com travamento mínimo e máximo. Tamanhos: 2,3mm diâmetro x 230cm comprimento. Agulha: 0,7mm diâmetro x 4,0mm ou 5mm comprimento.
a- Solução de adrenalina 1:10.000 (1ml 1:1.000 em 9ml de NaCl0,9%): punciona o território do vaso sangrante e injeta um volume o suficiente (pode chegar a 20ml) para provocar importante inchaço local com o objetivo não só da vasoconstrição da adrenalina, mas da consequente compressão do vaso sanguíneo pelo efeito mecânico. O efeito dura em torno de 24 horas, tempo suficiente para a trombose do vaso, na ausência de coagulopatia.
b- Solução de Etanolamina (Ethamolin®) 2%+ glicose a 50% ou álcool absoluto: neste caso é necessário identificar o ponto sangrante para injetar pequenos volumes (1 a 4 ml) somente em cima do vaso, para evitar aumentar a lesão e a reduzir o risco da perfuração. Posiciona a agulha tangencialmente à parede do cólon para que a solução seja injetada na submucosa quando ocorre a formação da “bolha”. A injeção na camada muscular pode acarretar perfuração tardia.
2- Terapia com Cauterização: cauterização bipolar e monopolar com heater probe e cauterização com gás de argônio
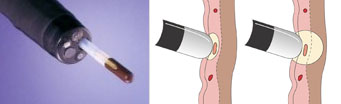
a- Cauterização monopolar com heater probe (sonda): a sonda é pressionado contra o ponto sangrante, interrompendo o fluxo de sangue, incialmente através da pressão e por fim pela cauterização. Não tem sido recomendado devido à profundidade da cauterização, mesmo mais superficial que a sonda monopolar comum, existe o risco de perfuração.

b- Cauterização bipolar: também de contato com efeito semelhante ao primeiro, mas a sonda bipolar impede a fuga de calor reduzindo a penetração tecidual e concentrando a cauterização no ponto sangrante, reduzindo significativamente o risco de perfuração.
 c- Cauterização com gás de argônio: A eletrocoagulação com argônio (APC) é um método de cauterização eletrocirúrgico, monopolar, no qual é aplicada uma corrente de energia de alta frequência sem entrar em contato direto com o tecido. Essa energia é levada ao tecido pelo gás argônio ionizado. O risco de perfuração praticamente não existe.
c- Cauterização com gás de argônio: A eletrocoagulação com argônio (APC) é um método de cauterização eletrocirúrgico, monopolar, no qual é aplicada uma corrente de energia de alta frequência sem entrar em contato direto com o tecido. Essa energia é levada ao tecido pelo gás argônio ionizado. O risco de perfuração praticamente não existe.
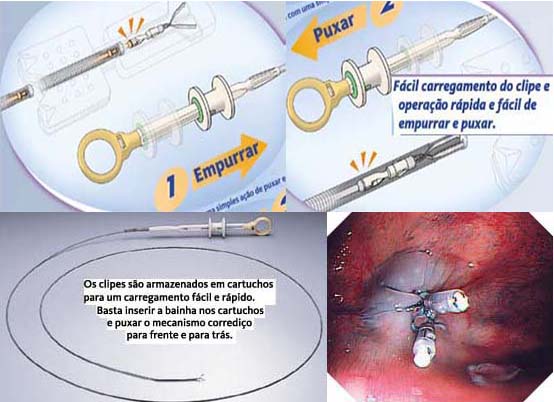 3- Métodos mecânicos: clipe metálico. O uso de hemoclip tem como pré-requisito para utilização a identificação do ponto de sangramento. Método mais eficaz e definitivo utilizado nas hemorragias de qualquer etiologia. Aplica-se um pequeno clip metálico estrangulando e obliterando, completamente, o vaso sanguíneo causador da hemorragia. O clip permanece aderido e é envolvido pelo tecido cicatricial. O material do clip é inerte em relação ao organismo.
3- Métodos mecânicos: clipe metálico. O uso de hemoclip tem como pré-requisito para utilização a identificação do ponto de sangramento. Método mais eficaz e definitivo utilizado nas hemorragias de qualquer etiologia. Aplica-se um pequeno clip metálico estrangulando e obliterando, completamente, o vaso sanguíneo causador da hemorragia. O clip permanece aderido e é envolvido pelo tecido cicatricial. O material do clip é inerte em relação ao organismo.
Doença Diverticular
Os divertículos são protrusões da mucosa através da parede do cólon, em pontos de menor resistência. É uma saliência parecida com a ponta de um dedo de luva.
Raramente antes da terceira década de vida, estima-se que aos 40 anos 5 a 10% e a partir da quinta década, mais de 50% após os 70 anos e 66% após a oitava. Não há predominância em relação ao sexo.
O sangramento é atribuído à lesão dos vasos que acompanham a herniação da mucosa (camada interna) que forma o divertículo. Fezes ressecadas presas dentro do divertículo podem machucar o revestimento interno (mucosa) e o vaso sanguíneo, causando o sangramento. Outra causa é o aumento progressivo do tamanho do divertículo e rompe o vaso. Ao evacuar, ao invés de fezes, sai grande quantidade de sangue vermelho vivo sem outros sintomas, geralmente em pessoas com mais de 60 anos hipertensos e/ou diabéticos.
É a principal causa de sangramento intestinal baixo volumoso, cerca de 50%. Mais comuns em pessoas com diabetes, arteriosclerose, hipertensão arterial e coagulopatia por doenças ou em uso de anticoagulantes (varfarina sódica).
A colonoscopia de urgência (primeira 24 horas de início do sangramento) é a principal arma para o tratamento dos casos que não melhoram com o tratamento clínico. Recomenda-se fazer o preparo intestinal (dose menor) e fazer o exame quando não estiver saindo fezes.
a – Solução de adrenalina 1:10.000 (1ml 1:1.000 em 9ml de NaCl0,9%): punciona o território do vaso sangrante e injeta um volume o suficiente (pode chegar a 20ml) para provocar importante ingurgitamento local com o objetivo não só da vasoconstrição da adrenalina, mas da consequente compressão do vaso sanguíneo pelo efeito mecânico. O efeito dura em torno de 24 horas, tempo suficiente para a trombose do vaso, na ausência de coagulopatia.
b – Cauterização bipolar: também de contato com efeito semelhante ao primeiro, mas a sonda bipolar impede a fuga de calor reduzindo a penetração tecidual e concentrando a coagulação no ponto sangrante reduzindo significativamente o risco de perfuração.
c – Métodos mecânicos: hemoclips metálicos. O uso de hemoclip tem como pré-requisito para utilização a identificação do ponto de sangramento. Método mais eficaz e definitivo utilizado nas hemorragias de qualquer etiologia. Aplica-se um pequeno clip metálico estrangulando e obliterando, completamente, o vaso sanguíneo causador da hemorragia. O clip permanece aderido e é envolvido pelo tecido cicatricial. O material do clip é inerte em relação ao organismo.
|
|
Ectasia Vascular Adquirida do Cólon
A ectasia vascular adquirida é a malformação vascular mais comum do cólon, geralmente entre 5 a 10 mm de diâmetro e múltiplas em 40 a 60% dos pacientes, mas tendem a se concentrar no mesmo segmento do cólon.
São alterações vasculares degenerativas adquiridas e decorre do envelhecimento da parede do intestino. Predominam em pessoas acima dos 60 anos, homens e mulheres, com pressão alta e/ou diabetes.
A abordagem das ectasias vasculares compreende três passos: diagnóstico da ectasia vascular como causa de sangramento; conversão da situação de urgência em eletiva (controle do sangramento); tratamento definitivo (endoscópico ou cirúrgico).
O achado casual de uma ectasia vascular em pacientes sem hemorragia digestiva baixa não determina necessidade de tratamento.
Alguns critérios são aplicados para definir a ectasia vascular como fonte de sangramento: detecção endoscópica de sangramento ativo oriundo da ectasia vascular; detecção de estigmas de hemorragia recente como coágulos, erosões ou sangue fresco próximo à ectasia vascular; paciente com hemorragia digestiva oculta, endoscopia digestiva alta e cápsula endoscópica ou enteroscopia normais, sendo, portanto a ectasia vascular não sangrante o único achado.
Definida a necessidade de tratamento, existem diversas modalidades terapêuticas usadas.
O tratamento endoscópico é o mais indicado. Existem diversas modalidades terapêuticas endoscópicas: eletrocoagulação com gás de argônio, eletrocoagulação bipolar ou “heater probe”, escleroterapia e ligadura elástica.
As complicações aumentam à medida que aumenta a profundidade da lesão causada por estas modalidades. A eletrocoagulação por “heater probe” é a terapia associada com maior profundidade e, portanto, maior número de complicações. 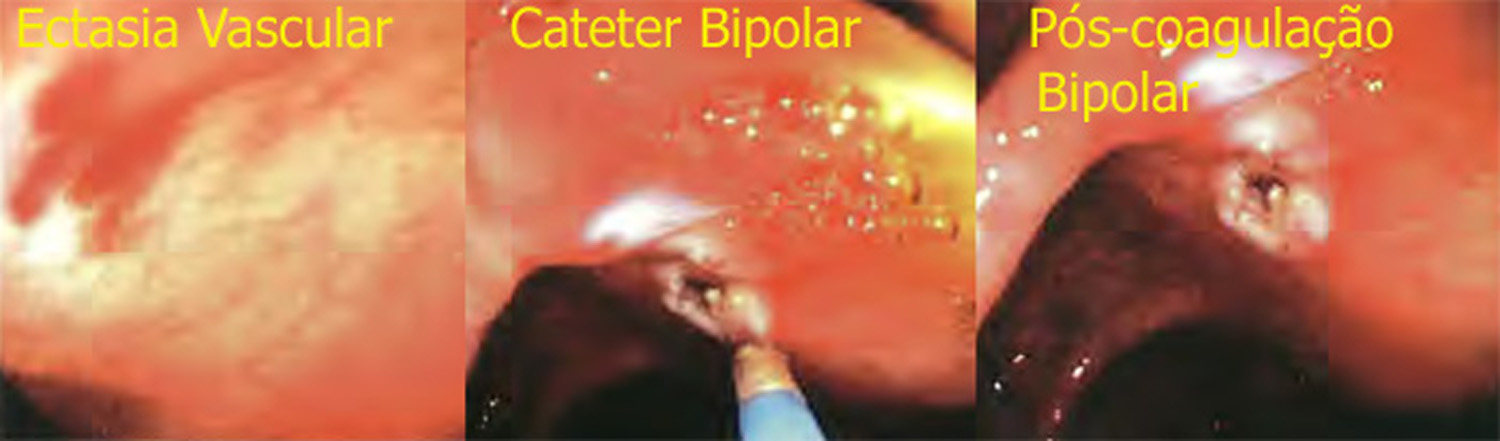
Sequência de tratamento com Coagulação Bipolar Sem Injeção na Submucosa: A – ecatasia vascular de 1 cm no ceco. B – coagulação bipolar em andamento. C – aspecto satisfatório após terapia com coagulação bipolar.
|
|
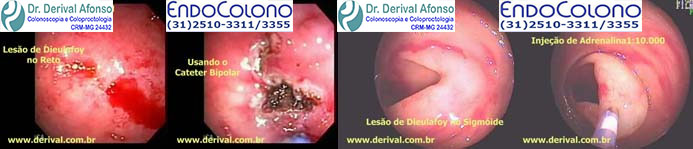
Lesão de Dieulafoy colorretal
A lesão de Dieulafoy é um vaso submucoso aberrante dilatado com calibre de 1 a 3 mm (aproximadamente 10 vezes o normal) que corrói a mucosa que o cobre na ausência de úlcera primária. As lesões de Dieulafoy do cólon são extremamente raras, em torno de 2%.
A etiologia da lesão de Dieulafoy é desconhecida. Além disso, eventos que desencadeiam os sangramentos não são bem compreendidos. Os pacientes que sangram das lesões de Dieulafoy são tipicamente homens com comorbidades, incluindo doença cardiovascular, hipertensão, doença renal crônica, diabetes ou abuso de álcool. O uso de AINEs também é comum entre pacientes com lesões de Dieulafoy; uma teoria é que os AINEs provocam sangramentos, causando atrofia das mucosas e lesões isquêmicas. Os episódios de sangramento geralmente são autolimitados, embora o sangramento possa ser recorrente e profuso.
A endoscopia é a modalidade diagnóstica de escolha para detectar a lesão de Dieulafoy e é particularmente útil quando realizada durante sangramento agudo. Isso ocorre porque o bombeamento arterial ativo pode ser visualizado em uma área sem úlcera ou lesão de massa associada Na ausência de sangramento ativo, a lesão de Dieulafoy pode aparecer como um mamilo aumentado ou vaso visível sem úlcera associada; no entanto, o vaso aberrante pode não ser visto, a menos que haja sangramento ativo no local. Como a lesão de Dieulafoy pode ser difícil de identificar, ela deve ser considerada no diagnóstico diferencial de sangramento sem uma fonte clara.
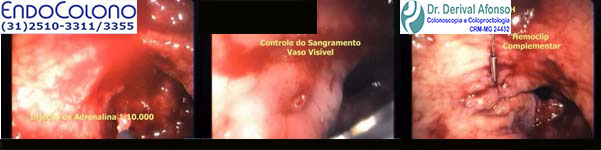
A hemostasia endoscópica pode ser obtida com uma combinação de injeção de adrenalina seguida de cauterização bipolar por sonda ou colocação de Clipe.
Outras abordagens usadas com sucesso no tratamento de lesões de Dieulafoy incluem cauterização por plasma de argônio e injeção de cianoacrilato.
A tatuagem endoscópica é útil para localizar a lesão para posterior retratamento endoscópico ou ressecção intra-operatória em cunha.
Se o ressangramento se repetir após um tratamento endoscópico, as opções terapêuticas incluem hemostasia endoscópica repetida, embolização angiográfica ou ressecção cirúrgica da cunha da lesão. Uma abordagem endoscópica e laparoscópica combinada foi descrita; essa abordagem permite a localização precisa da lesão com endoscopia intraoperatória, seguida de uma ressecção cirúrgica laparoscópica limitada da cunha. A ressecção cirúrgica deve ser reservada para sangramentos de difícil controle.
|
|
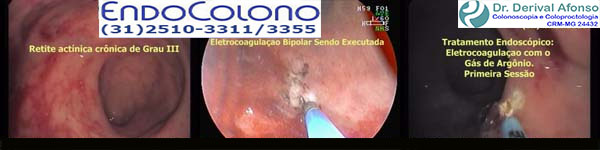
Retite Actínica Crônica (Proctopatia Actínica Crônica)
Lesões no reto provocadas pela radiação (irradiação) da radioterapia para tratamento de cânceres da bexiga, do reto, da próstata, dos testículos e ginecológicos.
Retite Aguda: quase 50% dos pacientes apresentam sintomas durante o tratamento da radioterapia pélvica. Retite crônica: em até 20% dos pacientes submetidos ao tratamento da radioterapia pélvica apresentará complicações em longo prazo. Além disso, entre 5 a 10% dos pacientes que desenvolveram lesão crônica do reto irão apresentar sangramento importante que requerem tratamento imediato com transfusões sanguíneas.
Irritação ou urgência retal e presença de muco e/ou sangue nas fezes, com ou sem evacuações frequentes com fezes amolecidas. A cauterização está indicada nos pacientes com sintomas moderados a graves que não responde ao tratamento clínico. O tratamento deve ser baseado no padrão e gravidade dos sintomas e na experiência do serviço.
Cauterização com gás de argônio. A cauterização com gás de argônio (APC) é um método de cauterização monopolar, no qual é aplicada uma corrente de energia de alta frequência sem entrar em contato direto com o tecido. Essa energia é levada ao tecido pelo gás argônio ionizado. Potência de 50Watt com fluxo de 2,0 l/min e pulso de 0,5s. Intervalo entre as sessões de 3 a 4 semanas.
A maioria dos pacientes apresenta melhora no sangramento e da anemia após uma média de 3 sessões. Todas as lesões vasculares visíveis devem ser cauterizadas em intervalos de quatro semanas. 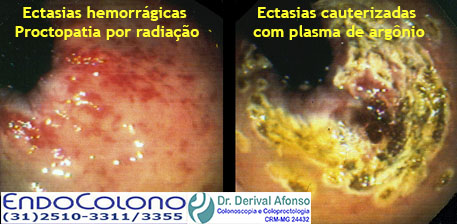
|
|
Eletrocoagulação bipolar. Disponível no serviço.
O equipamento necessário está amplamente disponível e é relativamente barato. A aplicação tangencial da sonda causa lesões superficiais cauterizando as ectasias da proctopatia por radiação. Pacientes com sangramento recorrente e anemia crônica devido a lesão induzida pela radiação são tratados, com números de sessões necessárias, até que o sangramento diminua significativamente. O resultado é confirmado pela melhora contínua do hematócrito.
Não existem grandes complicações. Cauterização endoscópica bipolar é executada com 10 a 15 W de potência usando a Probe de 7 Fr, pulsos de 2 segundos aplicadas nas ectasias vasculares até 2 cm da margem anal de forma radial.
|
|
Lesões com sinais de sangramento recente (coágulo aderido) ou ativo
Injeção de adrenalina associada à cauterização bipolar e/ou clipe endoscópico.
O uso de anti-inflamatório não esteroide, geralmente crônico e regular, pode causar úlceras, geralmente localizadas no ceco e cólon ascendente. As úlceras geralmente são arredondadas ou ovaladas, rasas e de bordas finas e pouco elevadas. A suspensão dos anti-inflamatórios pode resultar na regressão clínica e patológica resultando em cicatrização das lesões em semanas ou até meses.
Pacientes que se apresentam na forma aguda com sangramento são geridos de acordo com sua condição clínica. Podem ser diagnosticados e tratados pela colonoscopia, mas pode ser um desafio, uma vez que muitas vezes é difícil diferenciar de outras doenças, especialmente doença inflamatória intestinal e câncer. Ocorre em pacientes com mais de 50 anos (média de 61 anos) em ambos os sexos.
As informações contidas neste artigo são apenas para fins educacionais e não devem ser usadas para diagnóstico ou para orientar o tratamento sem o parecer de um profissional de saúde. Qualquer leitor que está preocupado com sua saúde deve entrar em contato com um médico para aconselhamento.
A colonoscopia é método eficaz no diagnóstico e tratamento dos doenças do íleo terminal, cólon e reto, sendo seguro e com baixo índice de complicações.
Biópsia (coleta de material para exame em laboratório).
Estudo dos pólipos pela colonoscopia.
Tratamento dos Pólipos pela Colonoscopia.
Técnicas usadas para retirar os pólipos por colonoscopia.
Tatuagem do cólon com tinta nanquim.
Complicações da polipectomia e mucosectomia.
Tratamento da hemorragia digestiva baixa (sangramento intestinal).
A colonoscopia é solicitada na suspeita de doenças do reto, cólon e íleo terminal. Solicitado também, para a prevenção do Câncer Colorretal. Permite a biópsia de alterações e a retirada dos pólipos. A maioria dos cânceres de intestino surge dos pólipos (adenoma ou serrilhado) que crescem no intestino e evoluem para o câncer. A lenta evolução dos pólipos, na maioria dos pacientes, permite que a colonoscopia os retire, evitando assim, o aparecimento do câncer e a possibilidade de morte. A colonoscopia encontra pólipos em até 30% das pessoas com 45 anos ou mais.
 Biópsia é um termo usado para descrever a remoção de uma amostra de tecido para enviar ao laboratório de anatomia patológica para análise. Para a biópsia na colonoscopia, uma pinça de biópsia é introduzida por dentro do aparelho até a sua extremidade final, permitindo retirar fragmentos (amostras) do tecido alterado e mesmo quando normal, se a indicação clínica recomendar e enviá-los para a análise em laboratório. As biópsias são usadas para identificar várias condições, mesmo que não se suspeite de câncer. A biópsia é sempre indolor.
Biópsia é um termo usado para descrever a remoção de uma amostra de tecido para enviar ao laboratório de anatomia patológica para análise. Para a biópsia na colonoscopia, uma pinça de biópsia é introduzida por dentro do aparelho até a sua extremidade final, permitindo retirar fragmentos (amostras) do tecido alterado e mesmo quando normal, se a indicação clínica recomendar e enviá-los para a análise em laboratório. As biópsias são usadas para identificar várias condições, mesmo que não se suspeite de câncer. A biópsia é sempre indolor.
|
|
Estudo dos pólipos pela colonoscopia
Uma vez identificado o pólipo, é necessário estudá-lo para definir se é possível a remoção por colonoscopia e qual é a melhor técnica a ser empregada. Avaliar se o aparelho está bem posicionado e de fácil manuseio para o tratamento imediato das complicações. É importante ter em mente os acessórios disponíveis para o procedimento proposto assim como para o tratamento das complicações.
Cromoscopia
Cromoscopia ou cromoendoscopia do cólon com índigo carmim a 0,2 a 0,5%. Consiste em aplicar um corante pelo canal do aparelho ou por cateter que em contato com a mucosa do cólon melhora a avaliação da superfície permitindo obter informações detalhadas da lesão, assim como do seu tamanho, limites e localização.
Deve ser aplicado com cuidado para não machucar a lesão e causar sangramento, o que dificultaria a avaliação. O corante recomendado no cólon e reto é o índigo carmim a 0,2 a 0,5%. A cromoscopia é usada para caracteriza melhor, delinear e realçar as lesões encontradas durante a colonoscopia. É importante limpar a superfície de lesões suspeitas retirando muco ou resíduos com água e às vezes com mucolíticos (N-acetilcisteína a 10%).
A cromoscopia pode ser utilizada de modo rotineiro, principalmente no ceco e cólon direito, para aumentar a chance de encontrar pólipos e lesões. Portanto, o mérito da cromoscopia é a determinação dos limites exatos da lesão, a visualização de partes ocultas e a demonstração de áreas deprimidas ou elevadas por meio do acúmulo e da distribuição do corante.
A videocolonoscopia convencional, sem magnificação de imagem, mesmo quando realizada por examinador experiente e com emprego de técnica de cromoscopia apresenta capacidade limitada de diferenciação de pólipos colorretais neoplásicos e não-neoplásicos. Quanto à diferenciação de pólipos colorretais benignos e malignos, não ocorreu nenhum caso de “subdiagnóstico. Algumas lesões benignas foram “superdiagnosticados” como malignas, o que, no entanto, não trouxe nenhum prejuízo uma vez que todos foram biopsiados.
Ao contrário da videocolonoscopia com magnificação de imagem, a videocolonoscopia convencional (sem magnificação de imagem) com cromoscopia é um exame diagnóstico de segurança limitada para determinação do diagnóstico histológico de lesões colorretais.
|
|
Magnificação de imagem pela colonoscopia
É a capacidade da colonoscopia em ampliar as imagens em tempo real (magnificação) permitindo a visualização de detalhes que não podem ser vistos com a colonoscopia padrão. As imagens podem ser aprimoradas ainda mais pelo uso de corantes (cromoscopia convencional) ou pelo próprio aparelho eletronicamente (cromoscopia eletrônica).
Os colonoscópios de magnificação possuem um mecanismo de foco ajustável que permite imagens endoscópicas padrão e a capacidade de ampliar a imagem de 1,5X a 200X.
O consenso entre observadores da análise da superfície das lesões é alto, mas não deve ser usada para decidir quais lesões colorretais devem ser retiradas ou não, uma vez que não se consegue diferenciar com precisão e segurança necessária as lesões neoplásicas (adenoma e serrilhado) das não-neoplásicas. Além disso, é baixa a capacidade em diferenciar as lesões neoplásicas não invasivas (câncer precoce) das neoplásicas invasivas (câncer avançado).
Os especialistas concordam que a colonoscopia com magnificação é útil, mas não substitui a avaliação histológica (biópsia) das lesões removidas.
|
|
Indicações da cromoscopia na colonoscopia
 A observação endoscópica com cromoscopia pode ser utilizada como método auxiliar em várias situações:
A observação endoscópica com cromoscopia pode ser utilizada como método auxiliar em várias situações:
– Estudo das lesões encontradas na colonoscopia convencional;
– Determinação com segurança das margens das lesões colorretais;
– Pesquisar lesão residual após as retiradas endoscópicas.
– No seguimento dos pacientes com doença inflamatória intestinal (doença de Crohn e retocolite ulcerativa) para avaliar o grau de atividade e prevenção do câncer colorretal.
Magnificação de imagem, permite a avaliação dos padrões de criptas da mucosa intestinal (pits), sendo a classificação de Kudo a mais utilizada. A classificação de Kudo subdivide o padrão de criptas em várias categorias (I, II, IIIL, IIIS, IV, Vi (irregular) e Vn (não-estrutural).
.
Todos os pólipos localizados no cólon e reto devem ser retirados pela colonoscopia ou cirurgia. A maioria dos pólipos é retirada pela colonoscopia com baixas taxas de complicações. Recomenda-se que os pólipos menores de 10 mm sejam retirados na introdução do colonoscópio, assim que identificados, porque existe o risco de serem perdidos na retirada do aparelho. A retirada de lesões maiores são trabalhosas e demandam mais tempo quando a injeção constante de ar para manter a luz aberta e retirar o pólipo pode dificultar o término do exame do exame. Para minimizar o risco de perda da lesão e a distensão exagerada do intestino, o local do pólipo pode ser marcado realizando duas biópsias, uma proximal e outra distal a lesão, facilitando a sua identificação e consequente a sua remoção na retirada do colonoscópio. 
|
|
De acordo com revisões sistemáticas e metanálises recentes, adenomas de baixo risco e adenomas avançados de alto risco são perdidos pela colonoscopia com mais frequência do que se acreditava anteriormente.
As perdas chegam a 27% para pólipos serrilhados, 26% para adenomas de baixo risco e 9% para adenomas avançados de alto risco (adenoma tubular ≥ 10 mm; adenoma viloso e displasia de alto grau). As taxas de perda são maiores para adenomas avançados proximais (cólon direito), pólipos serrilhados, adenomas planos e em pacientes com alto risco de câncer colorretal.
As taxas de perda podem ser reduzidas pela preparação adequada do intestino, exame cuidadoso dos ângulos e das pregas intestinais, distensão adequada da luz intestinal e tempo gasto para retirar o aparelho maior que 6 minutos. Atenção a pacientes com múltiplos pólipos e naqueles com histórico de pólipos, porque esses pacientes correm um alto risco de pólipos perdidos na colonoscopia.
Técnicas usadas para retirar os pólipos por colonoscopia
Pólipo séssil com até 3 mm de tamanho
A polipectomia com pinça fria é adequada para lesões com tamanho igual ou inferior a 3 mm. Idealmente, a lesão deve ser completamente envolvida pela pinça, sem tecido sobrando, para que toda a lesão seja removida em uma única mordida. Se ficar tecido residual, mordidas adicionais podem ser realizadas.
A vantagem desta técnica é que uma amostra é sempre recuperada para exame em laboratório. Outra vantagem consiste na não utilização do cautério com risco de sangramento e perfuração desprezíveis.
A desvantagem do uso da pinça é a dúvida sobre a remoção completa do pólipo. Em um estudo, 29% dos pacientes ainda apresentavam tecido neoplásico residual 3 semanas após o tratamento.

|
|
Pólipo séssil entre 3 e 9 mm de tamanho
Polipectomia com alça a frio, sem usar o cautério
A alça de polipectomia a frio é rápida, eficaz e segura e é a técnica preferida para pequenos pólipos sésseis de até 9 mm de tamanho. Para lesões maiores que 9 mm, pode ser difícil cortar o tecido com a alça sem cauterizar aumentando o risco de sangramento.
Uma alça de polipectomia pequena, mais rígida e fina e com abertura de menos de 12 mm é a ideal. A lesão deve ser colocada na posição das 5 horas, abre-se a alça e circunda o pólipo sem aspiração de ar. Então, a alça captura lentamente o pólipo com pelo menos 1 a 2 mm de tecido normal circundante. O pólipo é cortado, mas não deve ser levantado até que o fechamento da alça seja completo. O pólipo é aspirado através do canal de trabalho para um recipiente.
Taxas zero de perfuração e de menos de 2% de sangramento imediato, sem diferença quando comparado com os retirados com alça com cautério. Este sangramento é discreto e facilmente controlado com técnicas de hemostasia por colonoscopia.

|
|
Polipectomia com alça usando o cautério
Segue-se o mesmo procedimento descrito no uso da alça a frio, mas no momento de cortar o pólipo, utiliza-se a corrente elétrica produzida pelo cautério.
O cautério pode lesar a parede intestinal em graus variáveis e levar à síndrome pós-polipectomia e mesmo a perfuração. Portanto, deve ser usado com cautela em comparação com a alça a frio. Para minimizar este risco deve-se evitar apreender excesso de tecido normal e o pólipo laçado deve ser afastado da parede do cólon antes da aplicação da corrente elétrica. Atualmente, não há consenso sobre o tipo ideal de corrente que deve ser usado, mas geralmente utiliza-se corrente mista (blend).

|
|
Pólipo séssil maior ou igual a 10 mm e LST (lesão de crescimento lateral)
Ressecção Endoscópica da Mucosa – Mucosectomia
A ressecção endoscópica da mucosa (mucosectomia) é para lesões maiores que 15 mm e recomendado para 10 a 15 mm, mas alguns fazem a frio. Para lesões de 10 a 20 mm consegue-se, na maioria, a retirada em bloco e nas maiores de 20 mm recomenda-se o fatiamento para reduzir o risco de perfuração.
Consiste na injeção de soro fisiológico (NaCl 0,9%) com ou sem adrenalina (1:10.000 a 1:20.000) ou outras soluções abaixo da lesão para levantá-la, criando um plano protetor para colocar a alça de polipectomia e usar com certa segurança a corrente do eletrocautério (mista tipo blend 1). A lógica é facilitar a retirada endoscópica e potencialmente diminuir o risco de perfuração.
O pólipo deve ser orientado na posição das seis horas, que corresponde ao canal de trabalho do endoscópio. O pólipo é laçado e aplicado cauterização para ressecar o tecido.
Geralmente a solução é injetada no centro da lesão ou na borda proximal para que seja exposta. Antes de retirá-lo, é necessário definir as margens da lesão e na dúvida usa-se a cromoendoscopia convencional ou eletrônica com ou sem magnificação.
A falha no levantamento homogêneo da lesão com a injeção da solução suscita preocupação por malignidade, desde que o pólipo não tenha sido submetido a uma tentativa anterior de ressecção (o que poderia resultar em tecido cicatricial fixando a lesão na submucosa).
A injeção submucosa pode ter desvantagens.
—A solução salina é absorvida rapidamente e novas injeções pode dificultar laçar a lesão.
—O líquido injetado pode aumentar a tensão do tecido submucoso e dificultar a captura da alça (isto é, a alça desliza para fora do plano submucoso durante o fechamento).
—O líquido injetado pode se dissipar ao longo do plano submucoso, elevando o pólipo e a mucosa normal adjacente. Isso pode fazer com que o pólipo fique achatado ou deprimido em relação ao tecido circundante.
—A injeção pode deslocar a lesão para um local menos acessível, como atrás de uma dobra, ou contrair a luz, dificultando o acesso.
Após a ressecção, o local da polipectomia deve ter uma superfície “limpa”. A ressecção completa do pólipo em uma única sessão é fundamental, pois as cicatrizes dificultam uma segunda tentativa de ressecção.

|
|
A mucosectomia ideal é a que retira toda a lesão em um fragmento, ou seja, em bloco. As lesões com mais de de 20 mm essa ressecção em bloco pode ser difícil, além de aumentar o risco de complicações, principalmente a perfuração. Para essas lesões maiores de 20 mm, recomenda-se a retirada em fragmentos (mucosectomia a piecemeal).

|
|
Pólipos pediculados com pedículos com menos de 10 mm de diâmetro
São retirados com a alça de polipectomia usando o eletrocautério pela técnica simples
A técnica padronizada para remover esses pólipos pediculados consiste em abrir alça de polipectomia além da cabeça do pólipo recuando-a lentamente até laçar o pólipo. O pedículo deve ser laçado próximo à sua cabeça, com cuidado para garantir margem de segurança no caso de existir câncer associado e, ao mesmo tempo, um coto do pedículo residual visível que possa ser laçado no caso de sangramento.
Assim que a alça for fechada aplica-se a corrente mista (cauterização blend 1) para evitar o corte a frio e assim, reduzir a frequência de sangramento.
O coto residual do pedículo deve ser revisado alguns minutos após a polipectomia para assegurar a ausência de sangramento. O pólipo é recuperado e enviado para análise. Todo o processo é indolor.
As taxas de sangramento aumentam quando o pedículo é > 5 mm. No entanto, o tamanho para a aplicação de medidas profilática para evitar sangramentos não é conhecido. As diretrizes recomendam que, para um pólipo pediculado com uma cabeça ≥ 20 mm ou um pedículo ≥ 10 mm de diâmetro, usar medidas mecânicas para hemostasia e/ou usar uma injeção de adrenalina diluída.

|
|
Pólipos pediculados com pedículos entre 10 e 20 mm de diâmetro
As diretrizes recomendam que, para um pólipo pediculado com uma cabeça maior ou igual que 20 mm ou um pedículo entre 10 e 20 mm de diâmetro, usar uma injeção de adrenalina diluída profilaticamente.
Utiliza-se a mesma técnica recomendada para os pólipos menores, mas associado à injeção, em sua implantação na parede intestinal, de solução fisiológica (NaCl 0,9%) com adrenalina variando 1:10.000 a 1:20.000 (1 a 2 ml). Recomenda-se laçar o pedículo como descrito para os pólipos menores, mas mantendo o pedículo estrangulado por cerca de 4 a 5 minutos com o intuito de reduzir o fluxo sanguíneo e iniciar a cascata de coagulação e após este tempo procede-se a polipectomia como já descrito. Segue-se os mesmos cuidados após a polipectomia.
|
|
Pólipos pediculados com pedículos maiores de 20 mm de diâmetro
Estudos mostraram que pólipos com pedículos maiores que 20 mm de diâmetro têm um risco maior de sangramento imediato após a retirada (polipectomia). Nesses casos recomenda-se usar métodos profiláticos imediatamente antes da polipectomia para reduzir esse risco. O método ideal é o mecânico através do uso do endoloop (laço oval de nylon destacável) ou clip endoscópico metálico, isoladamente ou em combinação com injeção de adrenalina na base do pedículo. O endoloop e o clip endoscópico ficam presos no local, impedindo o sangramento.
O endoloop é colocado no pedículo do pólipo da mesma maneira que uma alça de polipectomia, mas depois de apertado é solto ao redor do pedículo. No entanto, existem problemas com os endoloops, como, por ser flexíveis, ter dificuldade em laçar o pólipo ou estrangular adequadamente, quando o sangramento imediato pode ocorrer. Sendo assim, o corte do pólipo com o eletrocautério deve ser realizado alguns minutos após o endolop ser apertado, tempo necessário para que o endoscopista perceba a alteração da cor da cabeça do pólipo de vermelho vivo para violáceo, demostrando diminuição significativa do fluxo de sangue.
Um ou mais clipes endoscópicos são colocados na base do pedículo imediatamente antes da polipectomia. A principal vantagem dessa abordagem é que os clipes endoscópicos geralmente são fáceis de colocar. As desvantagens incluem a frequente necessidade de usar vários clipes nos pedículos muito grandes e, de fato, pode ser inviável quando os clipes endoscópicos podem não ter tamanho suficiente para pegar todo o pedículo, mesmo quando vários clipes são aplicados. Outra desvantagem é o processo inflamatório que pode surgir em torno dos clipes que não caem dificultando a diferenciação com pólipo residual nas colonoscopias de controle.


|
|
Pólipos pediculados com a cabeça grande, maior que 25 mm
Quando identificado na introdução do colonoscópio, recomenda-se injetar em sua cabeça, solução com adrenalina variando 1:10.000 a 1:20.000. Reduz o fluxo de sangue e consequentemente o seu tamanho.
Na retirada do colonoscópio, quando provavelmente o pólipo já tenha ficado menor, realiza-se a polipectomia com ou sem a medidas profiláticas de sangramento usando o endoloop (laço oval de nylon destacável) ou clip endoscópico metálico, isoladamente ou em combinação com injeção de adrenalina na base do pedículo. Dependerá do julgamento do médico examinador.

|
|
Lesões Superficiais do Cólon
As lesões superficiais do cólon são as lesões nas quais o comprimento lateral e maior que a altura da lesão. Classificadas de acordo a sua forma em: superficialmente elevadas, deprimidas e de crescimento lateral.
O risco de evoluir para câncer é maior quando comparado a lesões elevadas (pediculada e séssil), mas o diagnóstico é mais difícil. Portanto, a identificação dessas lesões tem importância fundamental para a prevenção do câncer colorretal.
 Classificação de Paris
Classificação de Paris
ᴥ» Tipo IIa – lesão levemente elevada;
ᴥ» Tipo IIb – lesão completamente plana;
ᴥ» Tipo IIc – lesão levemente deprimida;
ᴥ» Tipo III – lesão ulcerada;
ᴥ» Tipo lla+llc – lesão levemente elevada com componente deprimido (tipo misto);
ᴥ» Tipo llc + lIa – lesão levemente deprimida com elevação nas bordas ou na parte central (tipo misto). Lesões planas elevadas (IIa) e lesões sésseis (Is) podem ser confundidas. A diferenciação se faz medindo a altura da lesão com a pinça de biópsia fechada, quando for mais elevada que pinça, isto é, maior que 2,5 mm é considerada séssil.
ᴥ» LST (lesão de crescimento lateral) – Considerada quando a lesão superficialmente elevada é maior que 10 mm. São classificadas em:
♦Lesão granular homogênea (nódulos pequenos);
♦Lesão granular mista (nodulações maiores e irregulares);
♦Lesão não granular plana;
♦Lesão não granular com componente deprimido.
Técnicas endoscópicas recomendadas para a retida (ressecção) das lesões superficiais do cólon
Tipo IIa menores que 2 cm. Tipo IIb menores que 1 cm
É usado a mesma técnica recomendada para os pólipos sésseis (alça de polipectomia a ᴥ» ᴥ» frio ou com eletrocautério ou a mucosectomia).
Tipo IIc, IIc+IIa e IIa+IIc menores que 1 cm
É usado sempre a técnica da mucosectomia em bloco (único fragmento). Exceto quando faltar a elevação da lesão ou a elevação da lesão for disforme com a injeção na submucosa (abaixo da lesão). Isso sugere câncer invasivo e impede o tratamento endoscópico. Nesse caso, faz-se a tatuagem alguns centímetros distais com tinta nanquim.
Tipo III – são lesões escavadas, isto é, do tipo ulcerado.
Apresentam uma alta incidência de câncer invasivo, independentemente do tamanho. Exceto quando faltar a elevação da lesão ou a elevação da lesão for disforme com a injeção na submucosa (abaixo da lesão). Isso sugere câncer invasivo e impede o tratamento endoscópico. Nesse caso, faz-se a tatuagem alguns centímetros distais com tinta nanquim.
LST (lesão de crescimento lateral)
A técnica de remoção, por colonoscopia ou por cirurgia, depende do tipo da lesão, da disponibilidade do serviço e da experiência da equipe.
Lesão entre 10 e 20 mm de tamanho
Ressecção endoscópica da mucosa (mucosectomia) em bloco único (EMR). Apenas quando o estudo da lesão pela cromoscopia com ou sem magnificação conseguir descartar áreas de câncer e a mesma se elevar por completo e de forma homogênea, após a injeção de solução na submucosa, sugerindo ausência de câncer invasivo.
 Lesão maior que 20 mm de tamanho
Lesão maior que 20 mm de tamanho
Ressecção endoscópica da mucosa em fragmentos – piecemeal – (EPMR) ou dissecção endoscópica de submucosa (ESD). O tamanho e forma da lesão, a experiência do endoscopista e o material disponível definem qual tipo de técnica usar.
Embora a ESD tenha um tempo de procedimento mais longo e uma maior taxa de perfuração, o seu uso fornece, frequentemente, uma ressecção em bloco.
No entanto, a técnica EPMR é considerada uma opção válida para ressecção de grandes lesões, uma vez que a ESD é pouco disponível. Na EPMR a presença de lesão residual (retirada incompleta) é de 16 % (geralmente uniforme e diminuto), enquanto a recorrência tardia é de 4%. Em ambos os casos se consegue o tratamento endoscópico em 93% dos casos.
Dissecção endoscópica de submucosa (ESD)
Permite a retirada de grandes lesões em bloco, através da criação de um plano na submucosa (camada entre a lesão de mucosa e a camada muscular). Esse plano é criado com a injeção de solução salina fisiológica (NaCl 0,9%) seguido da injeção da solução de absorção lenta como o HPMC (hidroxipropilmetilcelulosa) ou manitol, misturado com uma pequena quantidade de índigo carmim e adrenalina.
O corante índigo carmim facilita a visualização da camada submucosa e a adrenalina reduz o sangramento durante o procedimento. Um “cap” transparente é acoplado na ponta do endoscópio para ajudar na exposição durante o procedimento.
Inicia-se com a marcação da área ao redor da lesão através de pequenos pontos com o eletrocautério e assim delimitar os limites de ressecção embora alguns profissionais não a utilize. Na maioria dos casos, a incisão da mucosa é iniciada a partir da extremidade mais distante, para determinar o limite distal de ressecção.
Para usar a vantagem da gravidade, alterna a posição do paciente. Alterna-se a utilização dos acessórios de acordo com a necessidade durante o procedimento até a completa ressecção de lesões de praticamente qualquer tamanho.
Acessórios usados:
ᴥ» Para dissecção: I-T Knife II, Hook knife e Flex-knife;
ᴥ» Para hemostasia: pinça hemostática e HemoClips;
ᴥ» Para manter o cólon e reto distendido: bomba de CO2;
ᴥ» Para produzir a corrente de corte: bisturi elétrico de alta frequência com a função endocut o que propicia uma corrente pulsátil.
ᴥ» Para o colonoscópio: cateter injetor de água externa preso na ponta do aparelho por um “cap” transparente.

|
|
Tatuagem do cólon com Tinta Nanquim (tinta da índia)
A tatuagem consiste na injeção de um agente de coloração permanente na parede intestinal para criar uma marca que identificará o local de dentro ou de fora da luz; normalmente é feito com pelo menos duas injeções de corante nos lados contralaterais do intestino próximo à lesão.
A tatuagem deve ser realizada alguns centímetros distais à lesão. As duas principais indicações são:
ᴥ» Para marcar o local da retirada do pólipo, se não tiver certeza de que a remoção foi completa ou se serão necessárias outras sessões para removê-lo, se houver indicadores suspeitos de malignidade e para o controle de recidiva do pólipo, principalmente a retirado em mais de um fragmento (piecemeal).
ᴥ» Para identificar o local da lesão durante a cirurgia aberta e principalmente na laparoscópica e robótica (quando se perde o poder da palpação). A localização durante a cirurgia de lesões detectadas pela colonoscopia é imprecisa, quando se baseia na descrição da colonoscopia, levando em último caso, a não ressecção do segmento apropriado. No entanto, se a lesão estiver localizada no reto, no ceco ou próximo à válvula ileocecal, o local não precisa ser tatuado.
Cateter injetor – Produto tradicionalmente disponível para a injeção de outras soluções como de adrenalina ou ethamolin. Introduzido pelo canal de trabalho do aparelho, tem calibre ideal entre 23 – 25 G, com ponta de 3 – 5 mm.
Recomenda-se uma injeção dupla, com uma solução salina na submucosa para formar uma bolha, seguida de uma injeção de cerca de 1 ml da tinta nanquim esterilizada 1 a 5 % usando uma segunda seringa e completado com mais 1 a 2 ml de solução salina. Parece que esta técnica pode melhorar a eficácia da tatuagem e prevenir complicações inflamatórias e injeção na cavidade abdominal.
|
|
Complicações da polipectomia e mucosectomia
Geralmente são seguras quando realizadas por médico treinado e experiente. Complicações relacionadas: hemorragia, perfuração e a síndrome pós-polipectomia.
Hemorragia (sangramento)
A hemorragia é a complicação mais comum. O risco de sangramento é em torno de 1,7%. O sangramento pode ser imediato, imediatamente após (1,5%) ou tardio, ocorre em média 7 a 12 dias depois (2%). O sangramento varia de discreto em lençol a intenso e arterial, na forma de jato.
O risco está relacionado ao tipo e tamanho do pólipo, à técnica da polipectomia e ao status da coagulação do paciente. Em ambos os casos o tratamento endoscópico é o recomendado e consegue-se controlá-lo em quase todos os casos, sendo a cirurgia raramente necessária.
Tratamento pela colonoscopia no sangramento imediato após a retirada do pólipo
O sangramento imediato ocorre em 1,5% a 2,8% após polipectomia. O risco aumenta quando se descuida da técnica como usar uma corrente de corte muito forte e / ou ao fechar a alça muito rápido. Idade ≥65 anos, doença renal crônica ou cardiovascular, uso de anticoagulantes, pólipo maior que 1 cm de tamanho, morfologia do pólipo, mau preparo intestinal.
O sangramento mais imediato pode ser controlado com várias técnicas endoscópicas. A técnica depende da gravidade do sangramento, do tipo de pólipo e da preferência individual. Uma combinação de técnicas de hemostasia é frequentemente realizada.
Aplicação de pressão
Especialmente para pólipos pediculados, o sangramento imediato após a polipectomia pode ser facilmente interrompido através do controle do pedículo com a alça de polipectomia apertando o pedículo restante interrompendo o fluxo sanguíneo. Após a parada completa do sangramento ativo, outras técnicas devem sem usadas para reduzir o risco de novo sangramento como a cauterização bipolar, injeção de adrenalina ou uso do clip endoscópico.
Injeção com adrenalina
Uma diluição de epinefrina a 1: 10.000 é comumente usada, que é simplesmente injetada na área com sangramento. A injeção da adrenalina é frequentemente complementada com o clip endoscópico.
Cautério
 A cauterização é um método eficaz para tratar um local de sangramento. É feito com sondas térmicas, cauterização bipolar ou a ponta de uma alça de polipectomia. Como a parede do cólon é muito fina, a corrente deve diminuir em aproximadamente 50% em relação à usada no trato gastrointestinal superior. Para sonda de calor, 15 J é seguro e 10 a 15 W para cautério bipolar. Ao aplicar com sondas térmicas ou cautério bipolar, os endoscopistas não devem pressionar os dispositivos contra a lesão, o que aumenta o risco de perfuração.
A cauterização é um método eficaz para tratar um local de sangramento. É feito com sondas térmicas, cauterização bipolar ou a ponta de uma alça de polipectomia. Como a parede do cólon é muito fina, a corrente deve diminuir em aproximadamente 50% em relação à usada no trato gastrointestinal superior. Para sonda de calor, 15 J é seguro e 10 a 15 W para cautério bipolar. Ao aplicar com sondas térmicas ou cautério bipolar, os endoscopistas não devem pressionar os dispositivos contra a lesão, o que aumenta o risco de perfuração.
Clip endoscópico é um método seguro e eficaz para tratar sangramentos imediatos. Às vezes é difícil abordar uma lesão com clipes devido à localização. Estudo revelaram que são necessários uma média de 3 clipes para parar o sangramento completamente.
Endoloop e ligadura elástica
O sangramento pós-polipectomia imediato e tardio pode ser tratado com alças de endoloop ou ligadura da banda. Ao usar a ligadura de banda, deve-se evitar alta pressão de sucção para evitar perfuração.
|
|
Tratamento pela colonoscopia do sangramento tardio após a retirada do pólipo.
O sangramento tardio ocorre em até 2% dos pacientes que fizeram a polipectomia. Os sangramentos tardios se desenvolvem em média 5 a 7 dias após a polipectomia, mas podem ocorrer até 30 dias depois.
O tamanho do pólipo está relacionado ao risco de sangramento tardio de 1% para pólipos com menos de 10 mm a 6,5% para aqueles com mais de 20 mm. Idade avançada, hipertensão, pólipos sésseis grandes, pólipos no cólon direito e polipectomia com coagulação pura são conhecidos como fatores de risco para sangramento tardio. Anti-inflamatórios não esteróides ou aspirina não aumentam o risco de sangramento tardio.
A maioria dos sangramentos pós-polipectomia tardios podem ser tratados com sucesso com técnicas pela colonoscopia. Cerca de metade dos pacientes que são admitidos no hospital com sangramento intestinal dentro de 6 horas a 14 dias após a polipectomia requerem transfusão de sangue. O momento da intervenção depende da quantidade e da taxa de sangramento. A colonoscopia deve ser realizada imediatamente em pacientes com sangramento ativo. Injeção de adrenalina, terapia com eletrocautério ou clips endoscópcicos geralmente são realizados isoladamente ou em combinação.
SANGRAMENTO TARDIO APÓS-MUCOSECTOMIA – TRATAMENTO COM CLIP
|
|
Perfuração
A perfuração ocorre em 0,04% -2,1% quando se retira os pólipos (polipectomia ou mucosectomia).
Pode ser imediata ou tardia.
1- A perfuração imediata é causada por lesão de toda a parede do cólon ao retirar o pólipo.
2- A perfuração tardia ou em segundo tempo se deve a isquemia (falta de sangue) de toda a parede do cólon, ocorre em algumas horas ou dias após a retirada do pólipo.
A maioria das perfurações ocorre após a mucosectomia ou polipectomia de pólipos sésseis e subpediculados.
Dor abdominal associado a sinais de irritação peritoneal (piora da dor a qualquer atividade que mova ou tencione o abdome) após a retirada do pólipo é motivo de investigação imediata. Se o RX simples ou tomografia computadorizada do abdome mostrar ar livre (peumoperitôneo) confirma a perfuração, quando a cirurgia de urgência é mandatória.
Não se pode perder tempo, caso o médico considere a perfuração de vulto, por exemplo, através da visualização da cavidade abdominal ou de órgãos intra-abdominal, e a considera intratável por via colonoscópica.
Algumas perfurações podem ser fechadas imediatamente com clip endoscópico, nesses casos o paciente é internado e a cirurgia adiada. O paciente fica em jejum absoluto com antibióticos e soro por via intravenosa, as vezes usa-se sonda nasogástrica descompressiva, associado à observação clínica e laboratorial (leucograma e PCR) e acompanhado pelo cirurgião.
Com base em pesquisa disponível, na presença de ar livre abdominal (intraperitoneal ou retroperitoneal) sem notáveis sinais clínicos irritação peritoneal (“perfuração silenciosa”), a cirurgia pode ser adiada e com as mesmas medidas clínicas de quando se coloca o clip. As pequenas perfurações podem fechar espontaneamente sem a necessidade de terapia adicional invasiva.

|
|
Síndrome de coagulação pós-polipectomia
A síndrome de coagulação pós-polipectomia (também conhecida como síndrome pós-polipectomia, síndrome de eletrocoagulação pós-polipectomia e síndrome de queimadura transmural) refere-se ao desenvolvimento de dor abdominal localizada, febre e leucocitose (aumento dos leucócitos no sangue) na ausência de perfuração intestinal após a retirada de pólipos com eletrocautério.
O reconhecimento da síndrome de coagulação pós-polipectomia é importante para evitar cirurgia desnecessária, uma vez que o tratamento clínico é eficaz em quase todos os pacientes.
Ocorre em menos de 0,5% das colonoscopias com retirada de pólipos com eletrocautério. Fatores associados ao risco aumentado da síndrome:
ᴥ» Tamanho do pólipo – Quanto maior o pólipo (≥ 10 mm), maior o risco da síndrome;
ᴥ» Forma do pólipo – Lesão não polipóide tem um maior risco síndrome;
ᴥ» Localização da lesão – Lesões no cólon ascendente e no ceco parecem ter taxas mais altas de complicações, incluindo a síndrome pós-polipectomia, e isso se deve a espessura da parede intestinal ser menor;
ᴥ» Pacientes com hipertensão arterial – O risco é maior nos pacientes hipertensos.
Algumas técnicas endoscópicas podem reduzir o risco da síndrome de coagulação pós-polipectomia:
ᴥ» Tracionar o pólipo em direção ao centro da luz, imediatamente antes da aplicação do eletrocautério, para que a mucosa seja afastada do restante da parede intestinal;
ᴥ» Injetar de solução na submucosa para pólipos ≥ 10 mm;
ᴥ» Usar com mais frequência a polipectomia com alça a frio, sem usar o eletrocautério. Dados disponíveis sugerem ser uma opção segura e eficaz, mesmo para para lesões > 10 mm, localizadas no cólon direito e ceco.
Apresentação clínica
Tipicamente apresentam sintomas nas próximas 12 horas após a colonoscopia, mas podem ocorrer até sete dias depois. A maioria dos pacientes apresenta dor abdominal generalizada ou localizada na região do local da polipectomia. Febre e/ou taquicardia também podem estar presentes. O exame abdominal pode revelar sensibilidade abdominal localizada no local da polipectomia, mas alguns podem apresentar sinais e sintomas semelhantes a perfuração intestinal.
Diagnóstico
Deve-se suspeitar da síndrome de coagulação pós-polipectomia nos pacientes que apresentam dor e sensibilidade abdominal após a polipectomia com eletrocautério, particularmente após a remoção de pólipo grande (ou seja, ≥ 10 mm). Pode ser acompanhada por febre, taquicardia e leucocitose.
A tomografia computadorizada do abdome e da pelve (com contraste oral solúvel em água e contraste intravenoso) exclui a perfuração do cólon (ausência de ar livre no abdome). Podem ter espessamento focal da parede do cólon e/ou alteração da densidade da gordura em torno do cólon.
Para pacientes selecionados (por exemplo, aqueles com dor abdominal localizada leve, sem febre e sem taquicardia), pode ser razoável fazer o diagnóstico com base na apresentação clínica e sem exames complementares.
Tratamento
Pacientes selecionados podem ser tratados em regime ambulatorial se todas as condições a seguir forem atendidas:
ᴥ» Dor abdominal leve.
ᴥ» Pressão arterial, frequência cardíaca e respiratória normais e afebril.
ᴥ» Tomografia computadorizada abdominal e pélvica não mostra sinais de perfuração ou outras complicações graves.
O tratamento ambulatorial
Consiste no antibiótico oral por sete dias e uma dieta sem resíduos. Os pacientes são reavaliados clinicamente em dois a três dias. Se os sintomas melhorarem (por exemplo, sem dor abdominal ou febre), a dieta é liberada. Se a condição do paciente não melhorar ou piorar, a internação é necessária.
Antibiótico Oral
A queimadura da parede intestinal pode causar ruptura na barreira de defesa. Devem cobrir a flora gastrointestinal usual, bastonetes gram-negativos e anaeróbios.
ᴥ» Ciprofloxacino (500 mg de 12/12 horas) com metronidazol (500 mg de 8/8 horas).
ᴥ» Levofloxacino (750 mg ao dia) com metronidazol (500 mg de 8/8 horas).
ᴥ» Amoxicillina-clavulanato (875 mg amoxicillina e 125 mg clavulanato) de 8/8 horas. Dieta Dieta sem resíduos até que possam ser reavaliados em dois ou três dias. A dieta pode então ser liberada para uma dieta regular se melhorar clinicamente (sem dor ou sensibilidade abdominal).
Tratamento hospitalar
A hospitalização é necessária para os demais pacientes.
Dieta
Depende da gravidade dos sintomas, jejum (repouso intestinal completo) ou dieta sem resíduos. A resolução da dor abdominal ocorre em dois a três dias, quando a dieta é progredida.
Antibióticos venosos
A escolha depende da gravidade da doença. Metronidazol 500 mg IV cada 8 horas + Ceftriaxona 2g IV uma vez ao dia ou Cefotaxima 2g IV a cada 8 horas ou Ciprofloxacina 400 mg IV a cada 12 horas ou Levofloxacina 750 mg IV uma vez ao dia. Os antibióticos intravenosos devem ser continuados até que a dor abdominal desapareça, geralmente de dois a três dias, quando troca para antibióticos orais (por exemplo, ciprofloxacina com metronidazol ou monoterapia com amoxicilina-clavulanato), para completar um curso de sete.
Cuidados subsequentes
Pacientes com melhora clínica podem receber alta com antibióticos orais para completar um curso de sete dias. Critérios para a alta hospitalar: ᴥ» Normalização dos sinais vitais (isto é, resolução da febre, taquicardia e normalização da pressão arterial). ᴥ» Resolução de dor abdominal. ᴥ» Tolerância a dieta oral.
Pacientes que não melhoram
Se o paciente não melhorar ou piorar (por exemplo, aumento da dor abdominal ou leucocitose, ou desenvolvimento de peritonite difusa), é urgente a avaliação da cirurgia e nova tomografia computadorizada do abdome e da pelve é feita. Se houver suspeita de perfuração do cólon com base no exame clínico (por exemplo, defesa abdominal e rigidez) e/ou exames de imagem mostrando ar extraluminal, o tratamento é direcionado para a perfuração do cólon.
Introdução
 É o sangramento no trato digestivo que se origina abaixo do ângulo de Treitz (junção do duodeno com o jejuno). A saída de sangue vermelho vivo sem fezes através do ânus (enterorragia) tem sua origem no cólon, reto ou ânus em 85 a 90% dos casos.
É o sangramento no trato digestivo que se origina abaixo do ângulo de Treitz (junção do duodeno com o jejuno). A saída de sangue vermelho vivo sem fezes através do ânus (enterorragia) tem sua origem no cólon, reto ou ânus em 85 a 90% dos casos.
Predomina na terceira idade (acima dos 60 anos). Em cerca de 10% a origem não é encontrada.
ᴥ» Abaixo dos 60 anos: Doença diverticular do cólon; Doença inflamatória intestinal; Neoplasia; Ectasia Vascular. ᴥ» Acima dos 60 anos: Doença diverticular do cólon; Ectasia Vascular; Neoplasia.
Exame Clínico
História, exame clínico (frequência cardíaca, pressão arterial e cor das mucosas) e exame proctológico. Afasta doenças anorretais (neoplasias e orificiais – hemorroidas responde por 9% das causas) e também para confirmar o aspecto do sangramento relatado pelo paciente. A retossigmoidoscopia rígida pode ser realizada nos quadros estáveis, mas não elimina a necessidade de outros exames.
Exames Laboratoriais
Tipagem sanguínea, hemoglobina, hematócrito, uréia, creatinina, eletrólitos, glicemia atual e em jejum, coagulograma (TP, TTPA) e gasometria arterial. OBS: Hemoglobina imediata é de valor limitado na hemorragia aguda, pois são necessários de 24 a 48h para o organismo equilibrar o volume intravascular. Hemograma e coagulograma frequentes para avaliar necessidade de hemotransfusões e correção de coagulopatias.
Medidas Iniciais
ᴥ» A prioridade é garantir as vias aéreas pérvias.
ᴥ» Punção venosa no membro superior para coleta de sangue e infusão de soro fisiológico ou Ringer lactato e de concentrado de hemácias (hemotransfusão). O volume a ser infundido depende da perda estimada de sangue, da condição clínica e história de doença cardiovascular incluindo insuficiência cardíaca congestiva.
ᴥ» Correção da coagulopatia (RNI>1,5 – transfusão de plasma fresco e aqueles com contagem de plaquetas < 50.000 – transfusão de plaquetas) e dos distúrbios eletrolíticos se presentes.
ᴥ» Após 24 a 48 horas, com o equilíbrio do volume intravascular, o valor do hematócrito reduz-se. O hematócrito reduz-se aproximadamente 2 ou 3 pontos e a hemoglobina 1 ponto para cada 500 mililitros de sangue perdido. O objetivo é manter o hematócrito igual ou maior que 30 nos idosos e igual ou maior que 20 nos jovens saudáveis. ᴥ» A elevação da uréia/creatinina pode indicar gravidade do sangramento por refletir a intensidade da perda sanguínea e risco de insuficiência real aguda.
ᴥ» Sondagem gástrica para ver o conteúdo, quando não apresentam hematêmese (vômitos de sangue) e têm dificuldade de acesso à endoscopia para afastar origem gastroduodenal.
ᴥ» Acesso venoso central puncionando a veia jugular interna: para auxiliar a reposição volêmica e proporcionar a verificação periódica da pressão venosa central (PVC) nos casos de sangramento maciço e/ou instabilidade hemodinâmica
ᴥ» Colocação de cateter vesical: nos pacientes com choque hipovolêmico, para monitorar a resposta da reposição de fluídos por meio da perfusão renal.
Colonoscopia
A colonoscopia é o exame inicial de escolha na investigação e tratamento em pacientes com hemorragia digestiva baixa aguda moderada e maciça.
A acurácia diagnóstica varia de 72% a 86% com morbidade de 0,3%. O preparo de cólon anterógrado (via oral) é o método de eleição por ser fácil, útil e não causar ressangramento ou aumentar a velocidade do mesmo. Geralmente utiliza-se 50 a 75% da dose usual pelo sangue na luz intestinal ser um laxante natural.
O melhor momento para realizar a colonoscopia é em 12 a 24 horas após a chegada no hospital. Embora a colonoscopia de urgência realizada nas primeiras 12 horas seja segura e eficiente, e está relacionada à redução do tempo de internação e diminuição dos custos hospitalares.
Para a maioria dos profissionais a colonoscopia deve ser realizada assim que as condições clínicas, após as medidas iniciais, permitirem. Quando o sangramento é muito importante e não se consegue compensar adequadamente o paciente a colonoscopia deve ser realizada no CTI com o paciente intubado e 1 hora após o término do preparo de cólon através da sonda gástrica associado a 1000 ml de clister glicerinado.
Tratamento endoscópico na hemorragia digestiva baixa cólica
Métodos de tratamento endoscópico da hemorragia digestiva colorretal

1- Terapia com Infiltração: adrenalina, etanolamina e álcool absoluto Agulha de esclerose para colonoscopia com cateter em teflon e ponta afilada e sistema de manopla com travamento mínimo e máximo. Tamanhos: 2,3mm diâmetro x 230cm comprimento. Agulha: 0,7mm diâmetro x 4,0mm ou 5mm comprimento.
a- Solução de adrenalina 1:10.000 (1ml 1:1.000 em 9ml de NaCl0,9%): punciona o território do vaso sangrante e injeta um volume o suficiente (pode chegar a 20ml) para provocar importante inchaço local com o objetivo não só da vasoconstrição da adrenalina, mas da consequente compressão do vaso sanguíneo pelo efeito mecânico. O efeito dura em torno de 24 horas, tempo suficiente para a trombose do vaso, na ausência de coagulopatia.
b- Solução de Etanolamina (Ethamolin®) 2%+ glicose a 50% ou álcool absoluto: neste caso é necessário identificar o ponto sangrante para injetar pequenos volumes (1 a 4 ml) somente em cima do vaso, para evitar aumentar a lesão e a reduzir o risco da perfuração. Posiciona a agulha tangencialmente à parede do cólon para que a solução seja injetada na submucosa quando ocorre a formação da “bolha”. A injeção na camada muscular pode acarretar perfuração tardia.
2- Terapia com Cauterização: cauterização bipolar e monopolar com heater probe e cauterização com gás de argônio

a- Cauterização monopolar com heater probe (sonda): a sonda é pressionado contra o ponto sangrante, interrompendo o fluxo de sangue, incialmente através da pressão e por fim pela cauterização. Não tem sido recomendado devido à profundidade da cauterização, mesmo mais superficial que a sonda monopolar comum, existe o risco de perfuração.

b- Cauterização bipolar: também de contato com efeito semelhante ao primeiro, mas a sonda bipolar impede a fuga de calor reduzindo a penetração tecidual e concentrando a cauterização no ponto sangrante, reduzindo significativamente o risco de perfuração.
 c- Cauterização com gás de argônio: A eletrocoagulação com argônio (APC) é um método de cauterização eletrocirúrgico, monopolar, no qual é aplicada uma corrente de energia de alta frequência sem entrar em contato direto com o tecido. Essa energia é levada ao tecido pelo gás argônio ionizado. O risco de perfuração praticamente não existe.
c- Cauterização com gás de argônio: A eletrocoagulação com argônio (APC) é um método de cauterização eletrocirúrgico, monopolar, no qual é aplicada uma corrente de energia de alta frequência sem entrar em contato direto com o tecido. Essa energia é levada ao tecido pelo gás argônio ionizado. O risco de perfuração praticamente não existe.
 3- Métodos mecânicos: clipe metálico. O uso de hemoclip tem como pré-requisito para utilização a identificação do ponto de sangramento. Método mais eficaz e definitivo utilizado nas hemorragias de qualquer etiologia. Aplica-se um pequeno clip metálico estrangulando e obliterando, completamente, o vaso sanguíneo causador da hemorragia. O clip permanece aderido e é envolvido pelo tecido cicatricial. O material do clip é inerte em relação ao organismo.
3- Métodos mecânicos: clipe metálico. O uso de hemoclip tem como pré-requisito para utilização a identificação do ponto de sangramento. Método mais eficaz e definitivo utilizado nas hemorragias de qualquer etiologia. Aplica-se um pequeno clip metálico estrangulando e obliterando, completamente, o vaso sanguíneo causador da hemorragia. O clip permanece aderido e é envolvido pelo tecido cicatricial. O material do clip é inerte em relação ao organismo.
Doença Diverticular
Os divertículos são protrusões da mucosa através da parede do cólon, em pontos de menor resistência. É uma saliência parecida com a ponta de um dedo de luva.
Raramente antes da terceira década de vida, estima-se que aos 40 anos 5 a 10% e a partir da quinta década, mais de 50% após os 70 anos e 66% após a oitava. Não há predominância em relação ao sexo.
O sangramento é atribuído à lesão dos vasos que acompanham a herniação da mucosa (camada interna) que forma o divertículo. Fezes ressecadas presas dentro do divertículo podem machucar o revestimento interno (mucosa) e o vaso sanguíneo, causando o sangramento. Outra causa é o aumento progressivo do tamanho do divertículo e rompe o vaso. Ao evacuar, ao invés de fezes, sai grande quantidade de sangue vermelho vivo sem outros sintomas, geralmente em pessoas com mais de 60 anos hipertensos e/ou diabéticos.
É a principal causa de sangramento intestinal baixo volumoso, cerca de 50%. Mais comuns em pessoas com diabetes, arteriosclerose, hipertensão arterial e coagulopatia por doenças ou em uso de anticoagulantes (varfarina sódica).
A colonoscopia de urgência (primeira 24 horas de início do sangramento) é a principal arma para o tratamento dos casos que não melhoram com o tratamento clínico. Recomenda-se fazer o preparo intestinal (dose menor) e fazer o exame quando não estiver saindo fezes.
a – Solução de adrenalina 1:10.000 (1ml 1:1.000 em 9ml de NaCl0,9%): punciona o território do vaso sangrante e injeta um volume o suficiente (pode chegar a 20ml) para provocar importante ingurgitamento local com o objetivo não só da vasoconstrição da adrenalina, mas da consequente compressão do vaso sanguíneo pelo efeito mecânico. O efeito dura em torno de 24 horas, tempo suficiente para a trombose do vaso, na ausência de coagulopatia.
b – Cauterização bipolar: também de contato com efeito semelhante ao primeiro, mas a sonda bipolar impede a fuga de calor reduzindo a penetração tecidual e concentrando a coagulação no ponto sangrante reduzindo significativamente o risco de perfuração.
c – Métodos mecânicos: hemoclips metálicos. O uso de hemoclip tem como pré-requisito para utilização a identificação do ponto de sangramento. Método mais eficaz e definitivo utilizado nas hemorragias de qualquer etiologia. Aplica-se um pequeno clip metálico estrangulando e obliterando, completamente, o vaso sanguíneo causador da hemorragia. O clip permanece aderido e é envolvido pelo tecido cicatricial. O material do clip é inerte em relação ao organismo.
|
|
Ectasia Vascular Adquirida do Cólon
A ectasia vascular adquirida é a malformação vascular mais comum do cólon, geralmente entre 5 a 10 mm de diâmetro e múltiplas em 40 a 60% dos pacientes, mas tendem a se concentrar no mesmo segmento do cólon.
São alterações vasculares degenerativas adquiridas e decorre do envelhecimento da parede do intestino. Predominam em pessoas acima dos 60 anos, homens e mulheres, com pressão alta e/ou diabetes.
A abordagem das ectasias vasculares compreende três passos: diagnóstico da ectasia vascular como causa de sangramento; conversão da situação de urgência em eletiva (controle do sangramento); tratamento definitivo (endoscópico ou cirúrgico).
O achado casual de uma ectasia vascular em pacientes sem hemorragia digestiva baixa não determina necessidade de tratamento.
Alguns critérios são aplicados para definir a ectasia vascular como fonte de sangramento: detecção endoscópica de sangramento ativo oriundo da ectasia vascular; detecção de estigmas de hemorragia recente como coágulos, erosões ou sangue fresco próximo à ectasia vascular; paciente com hemorragia digestiva oculta, endoscopia digestiva alta e cápsula endoscópica ou enteroscopia normais, sendo, portanto a ectasia vascular não sangrante o único achado.
Definida a necessidade de tratamento, existem diversas modalidades terapêuticas usadas.
O tratamento endoscópico é o mais indicado. Existem diversas modalidades terapêuticas endoscópicas: eletrocoagulação com gás de argônio, eletrocoagulação bipolar ou “heater probe”, escleroterapia e ligadura elástica.
As complicações aumentam à medida que aumenta a profundidade da lesão causada por estas modalidades. A eletrocoagulação por “heater probe” é a terapia associada com maior profundidade e, portanto, maior número de complicações. 
Sequência de tratamento com Coagulação Bipolar Sem Injeção na Submucosa: A – ecatasia vascular de 1 cm no ceco. B – coagulação bipolar em andamento. C – aspecto satisfatório após terapia com coagulação bipolar.
|
|
Lesão de Dieulafoy colorretal
A lesão de Dieulafoy é um vaso submucoso aberrante dilatado com calibre de 1 a 3 mm (aproximadamente 10 vezes o normal) que corrói a mucosa que o cobre na ausência de úlcera primária. As lesões de Dieulafoy do cólon são extremamente raras, em torno de 2%.
A etiologia da lesão de Dieulafoy é desconhecida. Além disso, eventos que desencadeiam os sangramentos não são bem compreendidos. Os pacientes que sangram das lesões de Dieulafoy são tipicamente homens com comorbidades, incluindo doença cardiovascular, hipertensão, doença renal crônica, diabetes ou abuso de álcool. O uso de AINEs também é comum entre pacientes com lesões de Dieulafoy; uma teoria é que os AINEs provocam sangramentos, causando atrofia das mucosas e lesões isquêmicas. Os episódios de sangramento geralmente são autolimitados, embora o sangramento possa ser recorrente e profuso.
A endoscopia é a modalidade diagnóstica de escolha para detectar a lesão de Dieulafoy e é particularmente útil quando realizada durante sangramento agudo. Isso ocorre porque o bombeamento arterial ativo pode ser visualizado em uma área sem úlcera ou lesão de massa associada Na ausência de sangramento ativo, a lesão de Dieulafoy pode aparecer como um mamilo aumentado ou vaso visível sem úlcera associada; no entanto, o vaso aberrante pode não ser visto, a menos que haja sangramento ativo no local. Como a lesão de Dieulafoy pode ser difícil de identificar, ela deve ser considerada no diagnóstico diferencial de sangramento sem uma fonte clara.
A hemostasia endoscópica pode ser obtida com uma combinação de injeção de adrenalina seguida de cauterização bipolar por sonda ou colocação de Clipe.
Outras abordagens usadas com sucesso no tratamento de lesões de Dieulafoy incluem cauterização por plasma de argônio e injeção de cianoacrilato.
A tatuagem endoscópica é útil para localizar a lesão para posterior retratamento endoscópico ou ressecção intra-operatória em cunha.
Se o ressangramento se repetir após um tratamento endoscópico, as opções terapêuticas incluem hemostasia endoscópica repetida, embolização angiográfica ou ressecção cirúrgica da cunha da lesão. Uma abordagem endoscópica e laparoscópica combinada foi descrita; essa abordagem permite a localização precisa da lesão com endoscopia intraoperatória, seguida de uma ressecção cirúrgica laparoscópica limitada da cunha. A ressecção cirúrgica deve ser reservada para sangramentos de difícil controle.
|
|
Retite Actínica Crônica (Proctopatia Actínica Crônica)
Lesões no reto provocadas pela radiação (irradiação) da radioterapia para tratamento de cânceres da bexiga, do reto, da próstata, dos testículos e ginecológicos.
Retite Aguda: quase 50% dos pacientes apresentam sintomas durante o tratamento da radioterapia pélvica. Retite crônica: em até 20% dos pacientes submetidos ao tratamento da radioterapia pélvica apresentará complicações em longo prazo. Além disso, entre 5 a 10% dos pacientes que desenvolveram lesão crônica do reto irão apresentar sangramento importante que requerem tratamento imediato com transfusões sanguíneas.
Irritação ou urgência retal e presença de muco e/ou sangue nas fezes, com ou sem evacuações frequentes com fezes amolecidas. A cauterização está indicada nos pacientes com sintomas moderados a graves que não responde ao tratamento clínico. O tratamento deve ser baseado no padrão e gravidade dos sintomas e na experiência do serviço.
Cauterização com gás de argônio. A cauterização com gás de argônio (APC) é um método de cauterização monopolar, no qual é aplicada uma corrente de energia de alta frequência sem entrar em contato direto com o tecido. Essa energia é levada ao tecido pelo gás argônio ionizado. Potência de 50Watt com fluxo de 2,0 l/min e pulso de 0,5s. Intervalo entre as sessões de 3 a 4 semanas.
A maioria dos pacientes apresenta melhora no sangramento e da anemia após uma média de 3 sessões. Todas as lesões vasculares visíveis devem ser cauterizadas em intervalos de quatro semanas. 
|
|
Eletrocoagulação bipolar. Disponível no serviço.
O equipamento necessário está amplamente disponível e é relativamente barato. A aplicação tangencial da sonda causa lesões superficiais cauterizando as ectasias da proctopatia por radiação. Pacientes com sangramento recorrente e anemia crônica devido a lesão induzida pela radiação são tratados, com números de sessões necessárias, até que o sangramento diminua significativamente. O resultado é confirmado pela melhora contínua do hematócrito.
Não existem grandes complicações. Cauterização endoscópica bipolar é executada com 10 a 15 W de potência usando a Probe de 7 Fr, pulsos de 2 segundos aplicadas nas ectasias vasculares até 2 cm da margem anal de forma radial.
|
|
Lesões com sinais de sangramento recente (coágulo aderido) ou ativo
Injeção de adrenalina associada à cauterização bipolar e/ou clipe endoscópico.
O uso de anti-inflamatório não esteroide, geralmente crônico e regular, pode causar úlceras, geralmente localizadas no ceco e cólon ascendente. As úlceras geralmente são arredondadas ou ovaladas, rasas e de bordas finas e pouco elevadas. A suspensão dos anti-inflamatórios pode resultar na regressão clínica e patológica resultando em cicatrização das lesões em semanas ou até meses.
Pacientes que se apresentam na forma aguda com sangramento são geridos de acordo com sua condição clínica. Podem ser diagnosticados e tratados pela colonoscopia, mas pode ser um desafio, uma vez que muitas vezes é difícil diferenciar de outras doenças, especialmente doença inflamatória intestinal e câncer. Ocorre em pacientes com mais de 50 anos (média de 61 anos) em ambos os sexos.
As informações contidas neste artigo são apenas para fins educacionais e não devem ser usadas para diagnóstico ou para orientar o tratamento sem o parecer de um profissional de saúde. Qualquer leitor que está preocupado com sua saúde deve entrar em contato com um médico para aconselhamento.